- 国家市场监督管理总局
- 国家药品监督管理局
- 中国健康传媒集团主办
- 中央新闻网站
2025 年度医疗器械注册工作报告(摘登)
 |
|
 |
|
 |
|
 |
|
(上接6版)
注册的进口医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中21个子目录的产品。
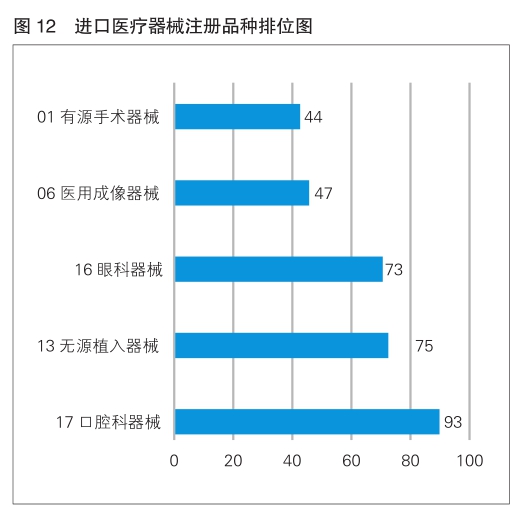
注册数量前五位的进口医疗器械是:口腔科器械、无源植入器械、眼科器械、医用成像器械、有源手术器械(见图12)。与2024年相比,变化较大,口腔科器械超过无源植入器械,位居第一,注册数量同比增加24%;眼科器械超过有源手术器械,注册数量同比增加35.2%;医用成像器械超过有源植入器械,进入前五位;其他品类注册数量略有下降。
(五)进口医疗器械国别情况
2025年,共有30个国家(地区)产品在我国获批上市。
其中,美国、德国、韩国、日本、法国医疗器械在我国医疗器械进口产品首次注册数量位列前五位,注册产品数量约占2025年进口产品首次注册总数量的75.4%。
从进口医疗器械代理人分布看,共有19个省份涉及有本省份企业作为进口医疗器械代理人,其中上海市代理人代理的进口首次注册医疗器械数量最多,占全部进口医疗器械数量的62.1%。
(六)境内第三类医疗器械省份分析
从2025年境内第三类医疗器械注册情况看,相关注册人主要集中在沿海经济较发达省份。
其中,江苏、广东、北京、上海、浙江是境内第三类医疗器械首次注册数量排前五名的省份,占2025年境内第三类医疗器械首次注册数量的65.1%。
四、创新医疗器械等产品注册审批情况
2025年,国家药监局按照《创新医疗器械特别审查程序》《医疗器械优先审批程序》继续做好相关产品的审查工作,共收到创新医疗器械特别审查申请457项,其中104项获准进入创新医疗器械特别审查程序;收到优先审批申请38项,其中26项获准优先审批。
从2014年至2025年,国家药监局共批准391个创新医疗器械上市。其中,境内创新医疗器械336个,涉及17个省份的223家企业;进口创新医疗器械55个,涉及6个国家的30个企业。北京、上海、江苏、广东、浙江创新医疗器械获批产品数量和相应企业数量最多,约占全部已批准的391个创新医疗器械的73.9%。
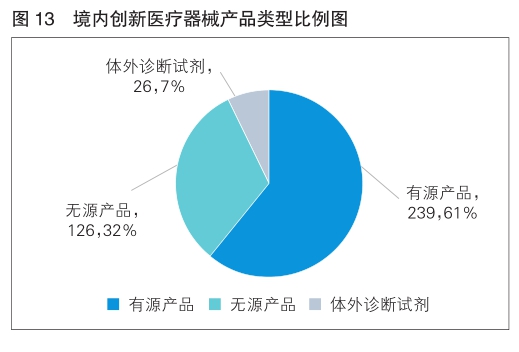
已批准的创新医疗器械中,有源产品占比约61%,无源产品约32%,体外诊断试剂产品约7%,具体见图13。
2025年,国家药监局共批准76个创新医疗器械产品上市,相比2024年增加16.9%。其中有源医疗器械45个,无源医疗器械29个,体外诊断试剂2个。
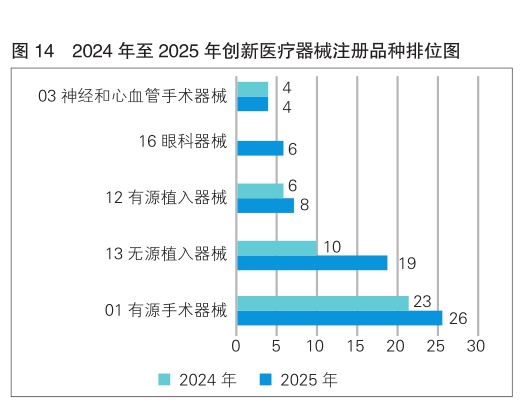
有源手术器械、无源植入器械、有源植入器械、眼科器械、神经和心血管手术器械是2025年批准的创新医疗器械数量前五位的品类,与2024年相比,无源植入器械和眼科器械品类的创新产品增长较快。具体见图14。
五、其他注册管理情况
(一)境内第二类医疗器械注册审批情况
2025年,各省级药品监管部门共批准境内第二类医疗器械注册41925项。其中,首次注册14466项,占全部境内第二类医疗器械注册数量的34.5%;延续注册14060项,占全部境内第二类医疗器械注册数量的33.5%;变更注册13399项,占全部境内第二类医疗器械注册数量的32%。2025年,各省份共注销1857个注册证。
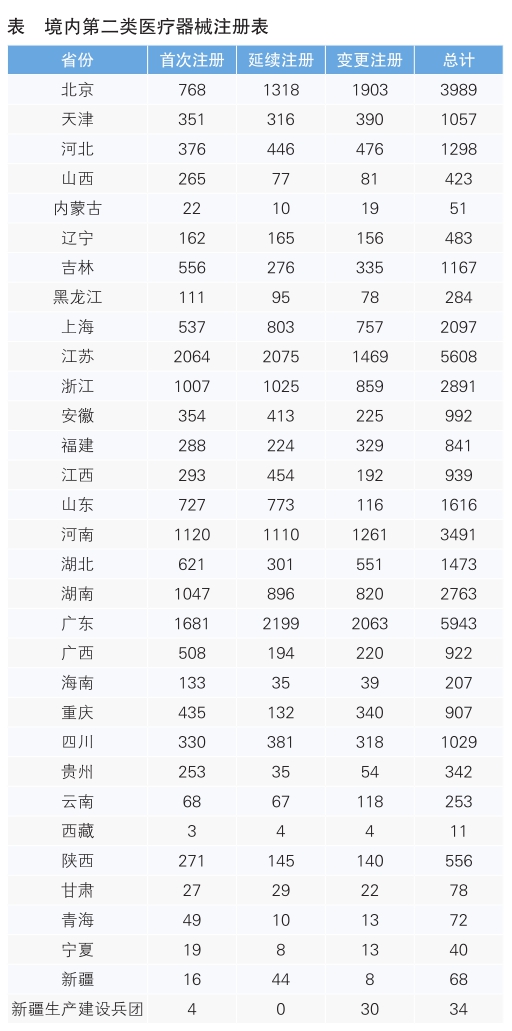
从注册情况看,广东、江苏、北京、河南、浙江、湖南、上海、山东、湖北、河北10省(市)办理境内第二类医疗器械注册事项较多。
第二类医疗器械注册具体数据见表。
从首次注册情况看,江苏、广东、河南、湖南、浙江、北京、山东、湖北、吉林、上海10省(市)首次注册的境内第二类医疗器械数量较多。
(二)第一类医疗器械备案情况
2025年,国家药监局依职责共办理进口第一类医疗器械备案1826项。
2025年,全国设区的市级药品监管部门依职责共办理境内第一类医疗器械备案21574项。其中江苏、广东、山东、河南、浙江是第一类备案数量前五的省份。
(三)登记事项变更/变更备案情况
2025年,国家药监局依职责共办理进口第二、三类和境内第三类医疗器械变更备案6415项。
其中,境内第三类医疗器械变更备案4546项,进口第二类、三类医疗器械变更备案1869项。
各省级药品监管部门依职责共办理境内第二类医疗器械变更备案17741项。
(四)医疗器械临床试验机构备案情况
自2018年1月1日《医疗器械临床试验机构条件和备案管理办法》实施以来,全国共计1645个机构完成了医疗器械临床试验机构备案工作,2025年新增备案机构214个,比2024年增加14.29%。
其中,广东、浙江、山东、四川、河南临床试验机构备案数量居全国前五名。
注:本报告的数据统计自2025年1月1日至2025年12月31日。(来源:国家药监局网站)
©2019中国食品药品网京公网安备 11010802023089号 京ICP备17013160号-1
《中国医药报》社有限公司 中国食品药品网版权所有






