- 国家市场监督管理总局
- 国家药品监督管理局
- 中国健康传媒集团主办
- 中央新闻网站
中国新药注册临床试验进展年度报告(2024年)(摘登)
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
 |
|
编者按
近日,国家药监局药品审评中心发布《中国新药注册临床试验进展年度报告(2024年)》(以下简称《报告》)。《报告》显示,2024年,药物临床试验登记与信息公示平台登记临床试验总量高达4900项[以临床试验登记号(以下简称CTR)计],较2023年登记总量增长了13.9%。申请人完成首次试验登记用时进一步缩短,临床试验启动效率进一步提高。
今日本报摘登《报告》部分内容,供业界参考。
摘要
《报告》根据2024年度药物临床试验登记数据,从临床试验登记总体概况、各药物类型临床试验基本特征、实施情况及质量控制情况等方面进行汇总分析。
一、主要研究结果
新药注册临床试验数量 2024年,药物临床试验登记与信息公示平台登记临床试验总量达4900项(以CTR计),较2023年增长了13.9%。其中,新药临床试验(以受理号登记)数量为2539项,较2023年增长了9.3%。
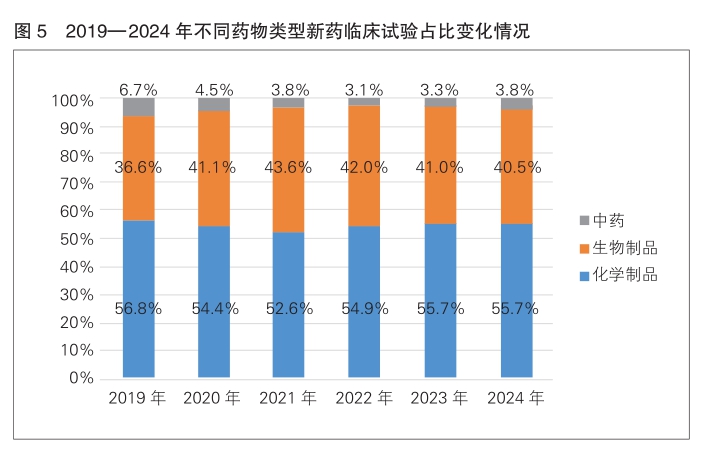
药物类型与注册分类 按化学药品、生物制品和中药分类,2024年化学药品和生物制品的新药临床试验占比较高,化学药品占比最高,为55.7%,生物制品占比约为40.5%,中药占比约为3.8%。
从注册分类分析,2024年注册分类为1类的药物共登记临床试验1735项,占新药临床试验(以受理号登记)总数的68.3%,其中化学药品占比最高,为52.3%。1类创新药临床试验以抗肿瘤药物占比较高,占总体的39.0%。
2024年细胞和基因治疗类产品共登记临床试验115项,较2023年增加了42.0%,以抗肿瘤适应证药物为主。医学影像学和放射性药物共登记临床试验23项,为近年来最多。
试验分类与申办者 按新药临床试验(以受理号登记)和生物等效性试验(BE试验)分类,2024年新药临床试验占比为51.8%,BE试验占比为48.2%。境内申办者占比为92.8%。
目标适应证与临床试验分期 2024年化学药品和生物制品临床试验的目标适应证主要集中在抗肿瘤领域,其次为皮肤及五官科药物、内分泌系统药物、神经系统疾病药物、呼吸系统疾病及抗过敏药物、预防性疫苗和血液系统疾病药物。中药主要集中在呼吸、消化等适应证。
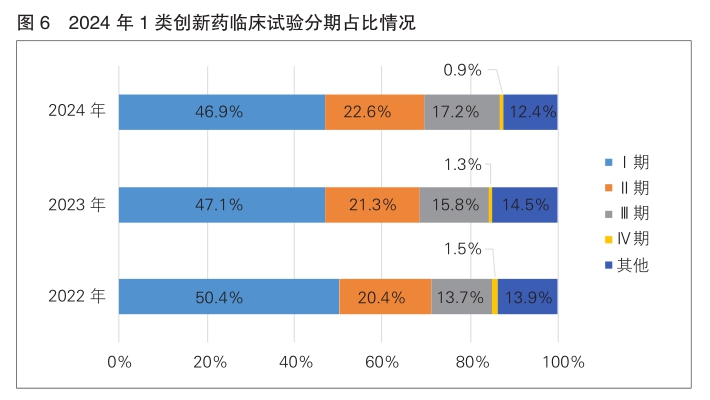
2024年登记临床试验中Ⅰ期临床试验占比最高,为39.9%。在1类创新药临床试验中,Ⅰ期临床试验占比为46.9%,Ⅱ、Ⅲ期临床试验占比相较上一年均出现小幅增加,分别为22.6%和17.2%。
在特定人群开展的临床试验中,2024年针对儿童人群开展的临床试验数量保持增长,达114项,其中Ⅲ期临床试验占比为43.9%。罕见疾病药物共登记临床试验121项,以血液系统疾病、神经系统疾病和抗肿瘤药物为主,占年度罕见疾病药物临床试验总量的63.6%。
临床试验地域分布分析 2024年临床试验组长单位和参加单位主要分布在北京市、上海市、江苏省、湖南省和广东省。儿童临床试验组长单位主要集中在北京市,广东省临床试验机构参与儿童临床试验的次数最多。
临床试验登记和实施效率分析 2024年,临床试验获批和BE备案后完成首次临床试验登记的平均用时分别为67.4天和12.1天,均较2023年进一步缩短;1个月以内完成试验登记并提交的占比分别为39.1%和91.7%,均较2023年进一步提高。
2024年,新药临床试验批准后的试验启动平均用时进一步缩短,在6个月内签署首例知情同意书的比例进一步提高,总体占比为65.5%。
若仅对临床试验获批后当年签署首例知情同意书情况进行分析,与2023年相比,2024年临床试验获批后的试验启动用时进一步缩短,6个月内签署首例知情同意书的比例仍保持增长,为96.9%。
二、结论
2024年临床试验登记总量保持增长,我国临床研发呈现积极态势。
药品注册分类以1类为主,Ⅱ、Ⅲ期临床试验占比均保持小幅增加。1类抗肿瘤创新药Ⅲ期临床试验保持小幅增长。罕见病临床试验数量和适应证领域均保持相对稳定。医学影像学和放射性药物临床试验数量保持小幅增加。细胞和基因治疗类产品临床试验数量较2023年增长明显。针对儿童人群开展的临床试验数量和在新药临床试验中的占比均保持增长,相关适应证主要为呼吸系统疾病及抗过敏和预防性疫苗。
申请人完成首次试验登记用时进一步缩短,临床试验启动效率进一步提高。
第一章
药物临床试验登记总体概况
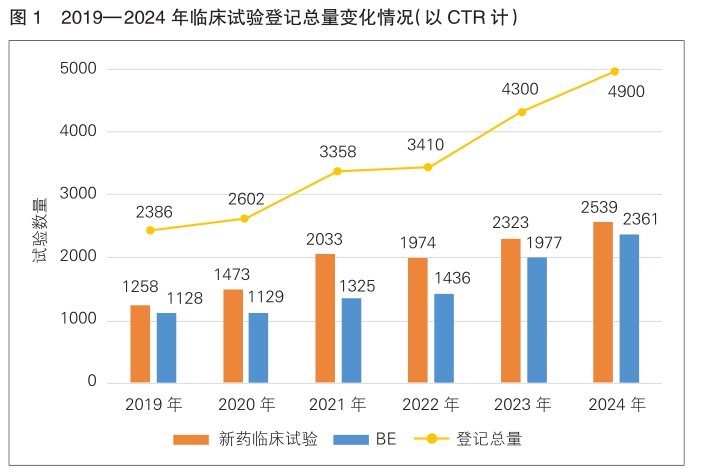
2024年中国药物临床试验年度登记总量为4900项(以CTR计,下同),与2023年相比增长了13.9%(4900vs.4300)。其中,以受理号登记的新药临床试验共2539项(51.8%,2539/4900),BE备案号登记临床试验共2361项(48.2%,2361/4900)。(详见图1)
按药物类型中药、化学药品和生物制品统计,2024年中国药物临床试验以化学药品为主,占比为76.9%;其次为生物制品,为21.1%;中药占比为2.0%。对比分析近年来数据,各类药物临床试验数量占比情况类似。
第二章
临床试验基本特征信息分析
一、药物类型及注册分类
中药 2024年共登记97项临床试验,主要以1类和原注册分类6类为主,占比分别为37.1%和36.1%,其次为2类,占比为15.5%。
化学药品 对于以受理号登记的新药临床试验,注册分类1类的药物占比最大,为64.3%,其次为2类,占比为20.7%。
生物制品 2024年治疗用生物制品以1类为主,占比为79.0%;预防用生物制品以1类和3类为主,占比分别为46.3%和20.9%。
二、目标适应证
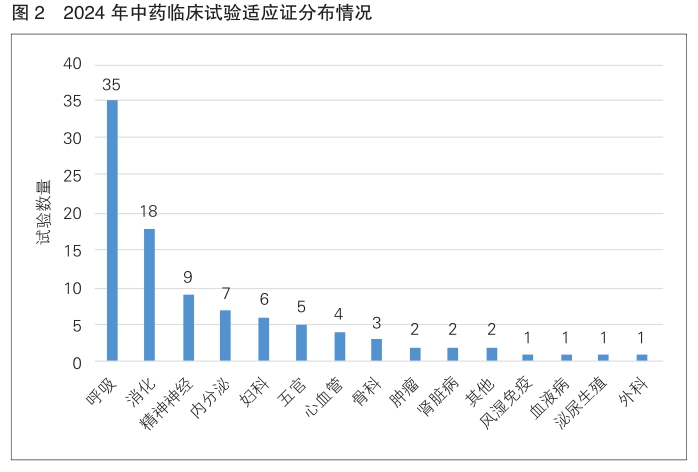
中药 2024年中药新药临床试验主要集中在呼吸和消化2个适应证领域,约占中药临床试验总体的54.6%,其中呼吸适应证占比最大,为36.1%。(详见图2)
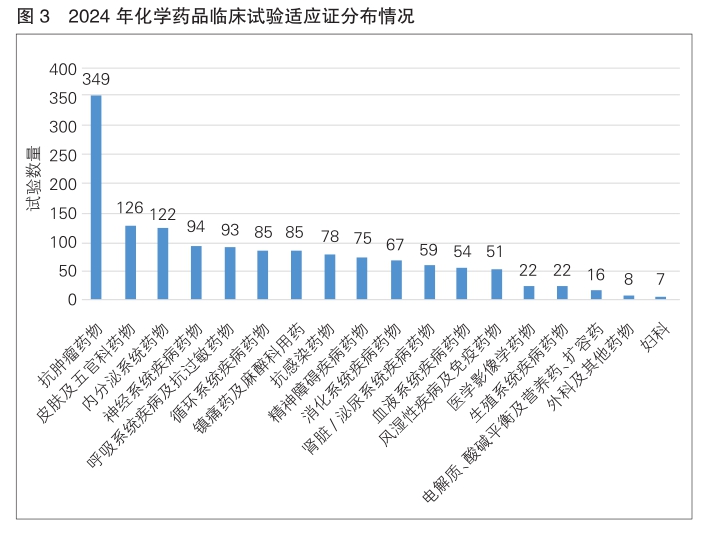
化学药品 2024年化学药品适应证以抗肿瘤药物为主,占化学药品临床试验总体的24.7%,其次分别为皮肤及五官科药物(8.9%)、内分泌系统药物(8.6%)、神经系统疾病药物(6.7%)和呼吸系统疾病及抗过敏药物(6.6%)。(详见图3)
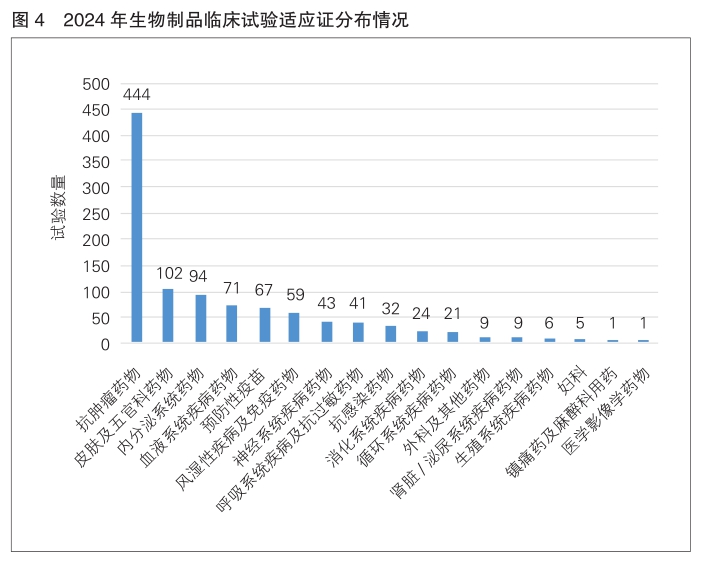
生物制品 2024年生物制品适应证同样以抗肿瘤药物为主,占生物制品临床试验总体的43.1%,其次分别为皮肤及五官科药物(9.9%)、内分泌系统药物(9.1%)、血液系统疾病药物(6.9%)和预防性疫苗(6.5%)。(详见图4)
三、临床试验类型与分期
1.新药临床试验
2024年以受理号登记的2539项新药临床试验中,化学药品、生物制品和中药分别登记1413项(55.7%)、1029项(40.5%)和97项(3.8%)。对比近年来新药临床试验登记数据,各类药物历年占比情况保持一致,均为化学药品最多(55.7%),其次为生物制品(40.5%左右)。(详见图5)
2.生物等效性试验及品种
2024年BE试验数量前10位品种中,富马酸伏诺拉生片登记试验数量最多,共67项。
3.临床试验分期
2024年,以受理号登记的2539项新药临床试验中,Ⅰ期占比为39.9%(1014项),Ⅱ期和Ⅲ期占比分别为19.5%(496项)和24.5%(622项),Ⅳ期临床试验有59项(主要为上市批件中明确要求开展的临床试验)。对于不能以Ⅰ、Ⅱ、Ⅲ、Ⅳ期独立划分的,按“其他”进行统计,如Ⅰ/Ⅱ期等。
与2023年相比,Ⅰ期临床试验占比略降,Ⅱ、Ⅲ期占比保持小幅增长。
对比近年来临床试验分期数据,各期临床试验占比总体稳定,其中Ⅰ期和Ⅲ期临床试验占比分别为40%和20%左右。
四、申办者类型
根据受理号对申办者类型进行分析,即受理号首字母为J的为境外申办者,其他为境内申办者。2024年登记的临床试验中,以境内申办者为主,占比为92.8%(4546项)。
第三章
各药物类型临床试验分析
一、新药临床试验及中化生品种概况
按照不同药物类型分别对2024年2539项新药临床试验所涉及的品种(按临床试验许可文件药品名称)数量进行统计。
中药 2024年共登记97项临床试验,约93.8%的中药品种在当年开展1项临床试验,开展2项临床试验的品种包括百蕊颗粒、加参片和小儿荆杏止咳颗粒。主动终止试验1项。
化学药品 2024年化学药品临床试验数量前10位品种共登记86项试验,占化学药品总体6.1%(86/1413),以司美格鲁肽注射液开展的试验数量最多,为14项。从适应证领域分析,前10位品种中内分泌系统药物试验共39项,涉及5个品种。
生物制品 2024年生物制品开展临床试验数量前10位品种共登记108项试验,占生物制品总体10.5%(108/1029),其中治疗用生物制品共涉及14个品种102项试验(94.4%),预防用生物制品涉及1个品种6项试验(5.6%)。抗肿瘤药物试验有56项(51.9%,56/108),涉及8个品种。
从单一品种临床试验数量分析,司美格鲁肽注射液开展临床试验数量最多,为15项。
二、1类创新药临床试验
根据注册分类对以受理号登记的2539项临床试验进行统计,2024年注册分类为1类(含原注册分类,下同)的药物共登记1735项试验,占总体的68.3%(1735/2539),其中化学药品占比最大,为52.3%(908/1735);其次为生物制品,为45.6%(791/1735)。
根据试验分期分析,Ⅰ期临床试验占比最高,为46.9%,Ⅱ、Ⅲ期临床试验占比分别为22.6%和17.2%。Ⅱ、Ⅲ期临床试验占比较2023年均出现小幅增加。(详见图6)
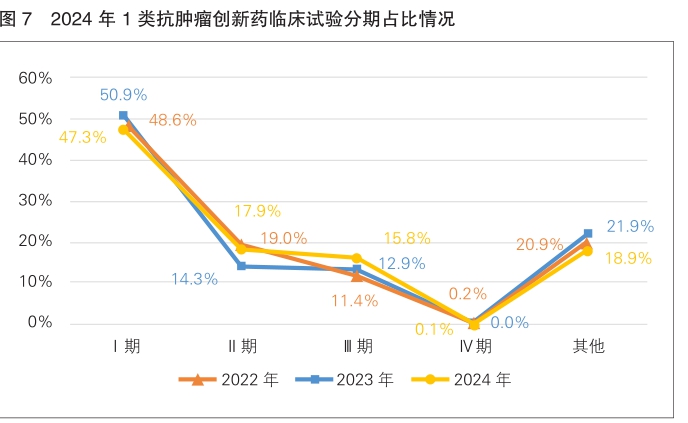
从适应证分析,1类创新药临床试验以抗肿瘤药物为主,占1类创新药总体的39.0%(677/1735),生物制品抗肿瘤药物占比高于化学药品,分别为50.1%(396/791)和30.9%(281/908)。结合试验分期分析,2024年1类抗肿瘤创新药Ⅲ期临床试验占比较2023年保持小幅增长,为15.8%。(详见图7)
(下转3版)
©2019中国食品药品网京公网安备 11010802023089号 京ICP备17013160号-1
《中国医药报》社有限公司 中国食品药品网版权所有






