□ 俞含莹 丁怡欣
近日,世界卫生组织(WHO)宣布猴痘疫情构成“国际关注的突发公共卫生事件”,引发广泛关注。世卫组织为猴痘拉响最高级别疫情警报等多个话题登上社交平台热搜榜。舆论聚焦猴痘疫情发展、变异新毒株突现,以及相关疫苗、治疗药物及检测试剂的研发进展等情况。
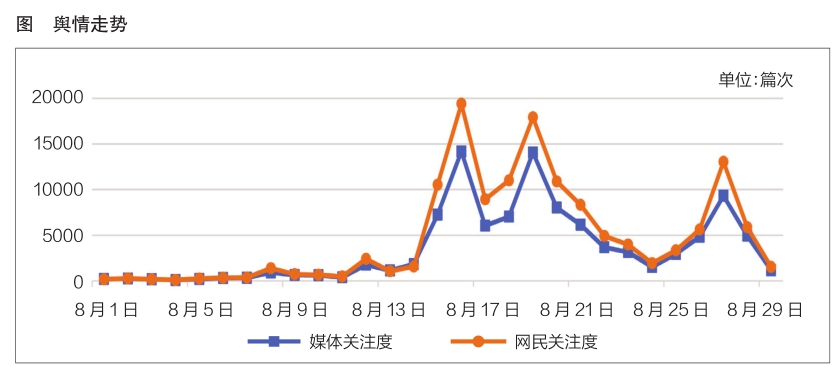
以2024年8月1日—29日为监测时间段,如图所示,舆情走势呈“波浪式”。8月16日,猴痘构成国际关注的突发公共卫生事件相关话题登上热搜,舆情达到最高峰。
猴痘疫情:卷土重来再拉警报
当地时间8月14日,WHO宣布,猴痘疫情构成“国际关注的突发公共卫生事件”。这是WHO三年来第二次就猴痘疫情拉响警报。2022年,猴痘Ⅱb变异株造成近200人死亡,WHO首次宣布猴痘疫情构成“国际关注的突发公共卫生事件”。直到2023年5月,WHO才解除这一状态。今年8月以来,猴痘疫情在非洲大面积暴发,时隔两年,世界卫生组织再次因猴痘疫情拉响最高警报。
警报拉响不久,就传来猴痘变异毒株突现的消息。央视新闻客户端发表《亚洲首例!猴痘变异新毒株出现,可飞沫传播!》一文称,近日,泰国出现首例猴痘Ib变异株病例,该变异病毒还可以通过分泌物(如呼吸道飞沫)、皮疹或受污染物品等方式进行传播。目前,我国尚无Ib变异株感染病例。
8月26日,WHO启动一项针对猴痘疫情的全球战略防范和应对计划,通过全球、地区和国家的协调努力遏制疫情传播。该计划包括针对猴痘疫情实施全面监测、预防和应对战略,推动研究和公平获取诊断检测工具和疫苗等医疗物资。该计划从今年9月持续至明年2月,预算为1.35亿美元。
猴痘疫情引发舆论广泛关注。世卫组织为猴痘拉响最高级别疫情警报、亚洲首例猴痘Ib变异病例出现等话题登上多个社交平台热搜榜。网民纷纷担忧病毒通过飞沫传播的风险,呼吁加强防控手段和措施。
媒体主要聚焦两个方面。
一是关注本轮猴痘疫情传播情况,以及与此前疫情相比有何不同。如新华网发表《非洲今年新增猴痘病例较去年同期激增160%》、中国新闻网发表《瑞典出现非洲以外首例猴痘新毒株感染病例》、央视新闻客户端发表《巴基斯坦今年已确诊3例猴痘病例》、环球网发表《菲律宾发现今年首例猴痘确诊病例》等文章对世界各地的猴痘病例情况进行报道。微信公众号“国家应急广播”发表《高度警惕!猴痘疫情扩散!世卫发布最高级别警报》一文称,本轮猴痘疫情相较两年前首波猴痘疫情存在两个主要差异:“分支I”毒株占比上升;受影响最大的人群是妇女和15岁以下的儿童。
二是关注防治猴痘疫情相关措施。新华网发表《世卫组织促增产猴痘疫苗 欧洲疾控中心上调感染风险级别》一文称,WHO敦促疫苗制造商增加猴痘疫苗产量,以控制一种更危险的猴痘毒株传播。同一天,欧洲疾病预防控制中心提高猴痘传播风险等级。此外,央视新闻等对我国海关总署、国家疾控局、国家卫生健康委出台的相关举措进行了报道。
疫苗:一款疫苗获WHO紧急使用授权
猴痘疫情卷土重来,疫苗需求迫切。猴痘疫苗的上市情况及研发进展成为舆论关注的焦点。
截至8月29日,世界卫生组织推荐的预防用猴痘病毒疫苗共3款,均为在预防天花的基础上获得猴痘预防/暴露后预防的批准/紧急使用。9月13日,WHO宣布,总部位于丹麦的巴伐利亚北欧公司所产猴痘疫苗为首个获紧急使用授权的猴痘疫苗。
国内方面,9月9日,国药集团中国生物上海生物制品研究所宣布,其自主研发的MVA株猴痘减毒活疫苗正式获得国家药监局签发的临床试验通知书。
人民日报健康客户端发表《我国猴痘疫苗距问世还有多远?》称,有多家生物药企以及科研机构开展了猴痘疫苗的研发工作,主要研发类型为复制缺陷型猴痘减毒活疫苗及猴痘mRNA疫苗。国药集团宣布研发了3种针对猴痘的候选mRNA疫苗。中山大学附属第七医院研发团队正开发多价猴痘mRNA疫苗。
另据媒体报道,智飞生物表示,公司在研管线内的猴痘疫苗产品处于临床前研究阶段。康希诺生物表示,公司已完成猴痘疫苗抗原初步筛选等前期工作,具备快速开发及制备疫苗的潜力及能力。
企业研发猴痘疫苗的同时,药监部门也在积极行动。8月26日,国家药监局药品审评中心就《预防用猴痘病毒疫苗药学研究评价技术要点(征求意见稿)》(以下简称《征求意见稿》)向社会公开征求意见。
治疗药物:药物有效性受质疑
2022年,欧洲药品管理局批准了美国SIGA公司研发的Tecovirimat(替韦立马)用于治疗天花、猴痘、牛痘。该药于2018年7月获美国食品药品管理局(FDA)批准上市,用于天花病治疗。但近期,Tecovirimat临床试验未及预期,引发不少媒体关注。智通财经发表《猴痘治疗药物Tecovirimat关键研究未达预期 SIGA盘前暴跌近40%》一文称,美国国立卫生研究院与刚果民主共和国国家生物医学研究所联合开展的关于抗猴痘病毒药物Tecovirimat的临床试验未能达到预期效果。在最新临床试验中,与安慰剂相比,Tecovirimat并未能显著缩短猴痘症状的持续时间。
在国内,部分药企正在抓紧研发针对猴痘的药物。据金融界报道,普利制药表示,目前国内尚未有全面的临床研究证明替韦立马和布林西多福韦这两种药物对猴痘病毒的治疗效果,其有效性仍需进一步论证。公司在研的替韦立马原料药及注射液、布林西多福韦原料药均尚在研发阶段,最终能否获批上市及获批时间仍存在不确定性。另据每日经济新闻报道,微芯生物表示,公司已有抗猴痘相关研发项目的储备,目前CDCS23项目已完成部分临床前工作,具有优异的抗病毒活性。
检测试剂:国内首款产品获批
自2022年首轮猴痘疫情开始,已有多家企业布局猴痘病毒检测试剂产品。国内外猴痘病毒检测试剂研发进展较疫苗、药物速度更快。南方网发表《国内首个猴痘病毒检测产品获批上市,由广东企业自主研发!》一文称,8月18日,国家药监局批准广州达安基因股份有限公司自主研发的猴痘病毒核酸检测试剂盒(荧光PCR法)上市。这是国内首个获批上市的猴痘病毒检测产品。
另有媒体关注到,多家A股上市公司已经布局了猴痘病毒检测产品。第一财经发表《猴痘疫情蔓延 多家公司回应相关业务情况》一文称,凯普生物表示,公司自主研发的猴痘病毒核酸检测试剂盒(荧光PCR法)已获欧盟CE证书,目前暂未取得国内医疗器械注册证,与猴痘病毒相关的发明专利已获国家知识产权局授权。乐普医疗表示,控股子公司北京乐普诊断科技股份有限公司自主研发、生产的猴痘病毒核酸检测试剂盒(PCR-荧光探针法)获得了欧盟CE注册证书。迈克生物表示,公司猴痘病毒核酸检测试剂盒(荧光PCR法)及猴痘病毒核酸检测试剂盒(数字PCR法)两款产品已取得欧盟CE准入资质。
微信公众号“体外诊断网”发文称,据业内不完全统计,目前国内研发猴痘检测试剂和原料的企业已超百家。
不过,也有观点认为,猴痘检测试剂盒的未来前景取决于多个因素,包括疫情发展、市场需求、技术创新和政策支持等,目前还很难研判收益如何。