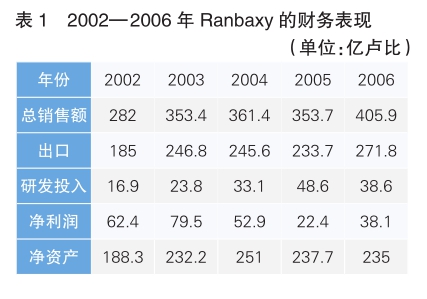
2000年后,欧洲各国大力推进仿制药替代,Ranbaxy的业务版图开始向欧洲扩张。为加快业务扩张速度,Ranbaxy将“持续评估在印度、新兴市场和发达市场的收购机会”纳入战略蓝图,先后收购了拜耳仿制药业务和RPG(安万特的业务部门),成为德国和法国主要仿制药企业之一。2004—2006年,Ranbaxy收购了11家企业,其全球仿制药巨头的地位逐渐形成,2006年总营收达到478亿卢比(详见表1)。
三、阴沟里翻船
2000年后,Ranbaxy面临的形势一片大好。该企业因为声称能够绕开立普妥专利向美国食品药品管理局(FDA)提交ANDA申请而引起轰动,甚至有美国龙头药企的印裔高管放弃了在美国企业的职位,回到印度投奔Ranbaxy。2006年前后是Ranbaxy的鼎盛时期,其不仅获得了辛伐他汀的市场独占期,阿托伐他汀的专利挑战也获得阶段性成果,创新药业务初显苗头。因为这些利好,Ranbaxy更加野心勃勃,制定了“在21世纪10年代实现年销售额50亿美元”的宏伟目标。因为Ranbaxy的出色表现,其成功经验被称为“Ranbaxy模式”,并被广大印度制药企业纷纷效仿和学习。
然而,就在如日中天时,Ranbaxy却在阴沟里翻了船。2008年,美国FDA宣布,禁止进口Ranbaxy生产的30多种仿制药,理由是Ranbaxy旗下Dewas和Paonta Sahib两家工厂的生产过程不符合美国cGMP相关规定,存在交叉污染等问题。当时,美国是Ranbaxy第一大市场,Ranbaxy超过40%的销售额由美国市场贡献。FDA的警告让Ranbaxy光明的前景突然变得阴霾遍布。就在此时,第一三共以46亿美元的价格收购了Ranbaxy过半股权,控股了Ranbaxy。
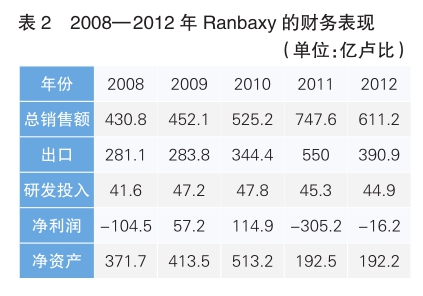
先收购不良资产,然后包装盘活是很多资本家惯用的手段,但第一三共在收购Ranbaxy股权的交易中并未捡到便宜,Ranbaxy的厄运也没有因为第一三共的收购而停止。因为美国FDA的禁令,2008年,Ranbaxy的销售额增速大幅下降,净亏损达105亿卢比(详见表2)。2009年,FDA在核查中发现,Ranbaxy的Paonta生产基地以往提交的ANDA申请中,使用了不真实材料,于是合规性问题上升为真实性问题。造假风波还未得到妥善解决,美国联邦调查局又以“长期销售掺假药物”为名对Ranbaxy展开调查,Ranbaxy不得不支付1.5亿美元的罚款和3亿美元的官司索赔。
事实上,Ranbaxy的造假问题长期存在。2000年以来,Ranbaxy向巴西提交的多份文件中都存在数据造假问题。2003年10月,多个国家药品监管部门的审查员开始对Ranbaxy的生产场地进行轮番调查。虽然Ranbaxy表面上积极为患者服务、为公益事业奉献,但内部早已动荡不堪,高管之间疲于争斗,漠视药品安全。2005年后,美国FDA加大了对Ranbaxy的检查力度,最终出现了上文所述情况。
因为造假问题,Ranbaxy此前备受期待的立普妥、代文等重磅炸弹首仿药的市场独占期资格化成了泡影,企业从此一蹶不振。
2013年,Ranbaxy的生产基地又一次曝出药品安全问题,产品被美国FDA禁止进口。Ranbaxy历经艰辛,花费近30年打造的出海之路毁于一旦。
2008—2013年,Ranbaxy合计净亏损额达342亿卢比。2014年,第一三共以40亿美元的价格将Ranbaxy“甩卖”给了太阳制药。 (二)
(摘编自《仿制药企兴衰启示录》,中国医药科技出版社出版)