根据药物临床试验登记与信息公示平台登记信息,截至2025年6月30日,我国共登记先进治疗药物临床试验427项。其中,Ⅰ期临床试验222项(52.0%);Ⅱ期临床试验58项(13.6%);Ⅲ期临床试验16项(3.7%);其他类型临床试验(由于填报信息不全或不规范而无法统计的试验)131项(30.7%)。
从完成情况来看,已完成的临床试验共24项。其中,Ⅰ期临床试验14项;Ⅱ期临床试验4项;Ⅲ期临床试验2项;其他类型临床试验4项。
临床试验启动与完成用时
以国内第一例受试者签署知情同意书的日期,作为先进治疗药物注册临床试验的启动节点。截至2025年6月30日,427项临床试验中有129项尚未更新第一例受试者知情同意书签署日期,或暂无受试者入组;其余298项临床试验启动最短用时16天,最长用时1938天。
已完成的24项临床试验整体耗时多在1年及以上。其中,完成用时最短为318天,最长为1548天。
当前正在开展的先进治疗药物临床试验以Ⅰ期为主,进入Ⅱ期及以后阶段的临床试验数量明显减少,提示Ⅰ期临床试验的推进效率与研发风险值得重点关注;同时,已开展临床试验的品种数量,不超过获批临床研究总量的85%,反映部分品种临床试验推进较慢。
临床试验设计和开展范围
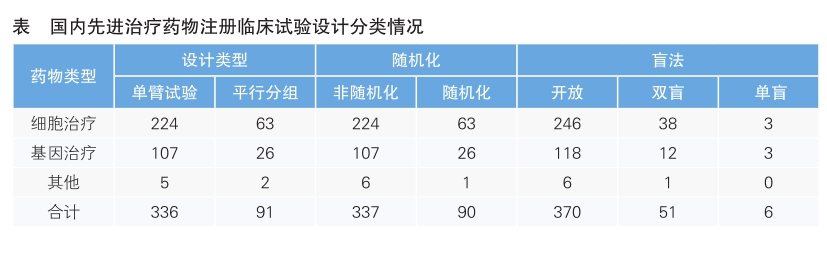
从已登记的427项先进治疗药物临床试验设计情况来看,336项为单臂试验,91项为平行分组;337项临床试验为非随机化,90项临床试验为随机化;370项临床试验为开放试验,51项临床试验为双盲,6项临床试验为单盲(详见表)。
我国先进治疗药物的临床试验,仍以境内开展为主,共413项;国际多中心临床试验仅14项。
申请人区域分布
承担先进治疗药物临床试验的申请人地域集中度较高。按药物类型细分,细胞治疗药物临床试验的申请人主要集中于上海、北京、广东。其中,上海96个,占比33.4%;北京59个,占比20.6%;广东28个,占比9.8%。基因治疗药物临床试验申请人排名前三的地区为上海、北京、湖北。其中,上海45个,占比33.8%;北京28个,占比21.0%;湖北14个,占比10.5%。其他类型先进治疗药物临床试验申请人所在区域以北京为主,共4个,上海、四川、湖北各1个。
整体而言,我国先进治疗药物研发高度集中于长三角、京津冀及珠三角等医药产业发达区域,中部及西南地区发展势头强劲,东北、西北等地区布局则相对滞后。
(摘编自《中国先进治疗药品研发现状与进展》,中国医药科技出版社出版)