第一章 药品注册申请受理情况
(一)总体情况
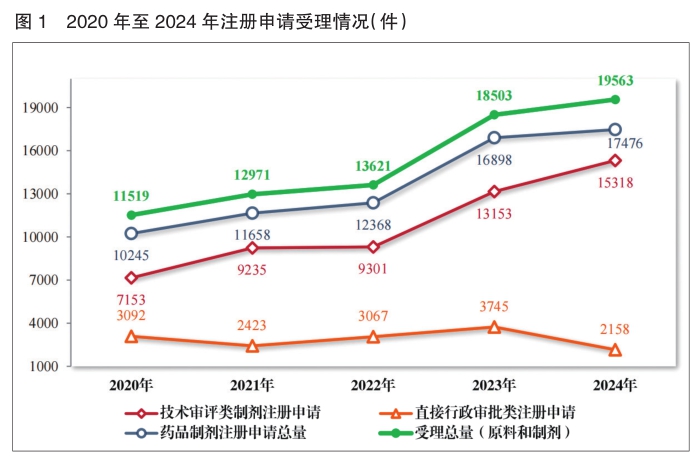
2024年,药品注册申请申报量持续增长,国家药监局药品审评中心(以下简称药审中心)受理各类注册申请19563件(同比增加5.73%,以受理号计,下同),包括药品制剂注册申请17476件(同比增加3.42%)、化学原料药注册申请2087件(同比增加30.03%)。17476件药品制剂注册申请包括技术审评类注册申请15318件(同比增加16.46%)、直接行政审批类注册申请2158件(包括补充申请和一次性进口)。
(二)技术审评类药品注册申请受理情况
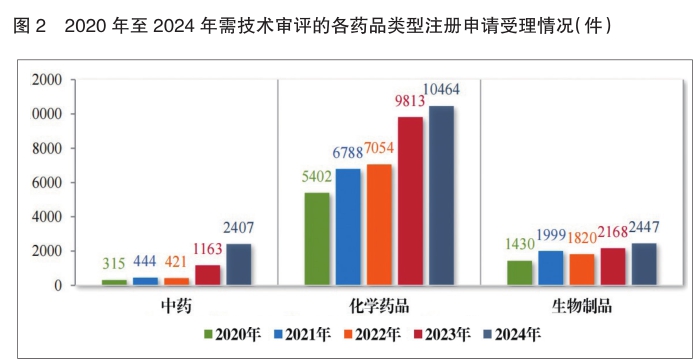
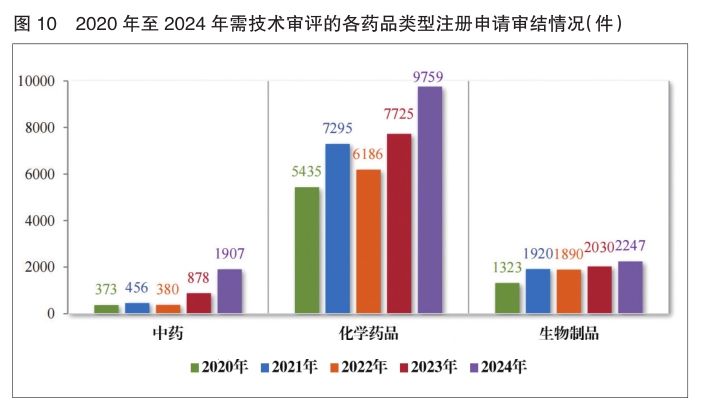
2024年受理的15318件技术审评类药品注册申请中,以药品类型统计,中药注册申请2407件、化学药品注册申请10464件、生物制品注册申请2447件。
以注册申请类别统计,受理新药临床试验申请(该注册申请类别以下简称IND)3073件,验证性临床试验申请247件,新药上市许可申请(该注册申请类别以下简称NDA)549件,同名同方药、化学仿制药上市许可申请(该注册申请类别以下简称ANDA)4770件,仿制药质量和疗效一致性评价注册申请(该注册申请类别以下简称“一致性评价申请”)659件,补充申请5600件,境外生产药品再注册申请420件。
1.中药注册申请受理情况
2024年受理中药注册申请2407件,按注册申请类别统计,IND 100件,NDA 40件,补充申请2262件,ANDA 2件,境外生产药品再注册申请3件。
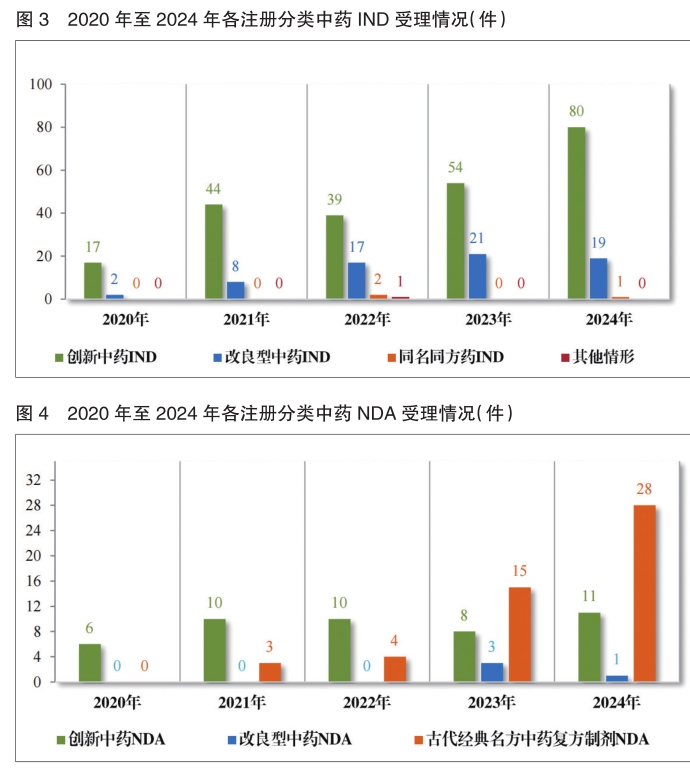
以注册分类统计,100件IND中,包括创新中药IND 80件(71个品种)、改良型中药IND 19件(16个品种)、同名同方药IND 1件(1个品种);40件NDA中,包括创新中药NDA 11件(11个品种)、改良型中药NDA 1件(1个品种)、古代经典名方中药复方制剂NDA 28件(17个品种)。
2.化学药品注册申请受理情况
2024年受理需技术审评的化学药品注册申请10464件,按注册申请类别统计,IND 1785件,验证性临床试验申请247件,NDA 255件,ANDA 4768件,一致性评价申请659件,补充申请2396件,境外生产药品再注册申请354件。
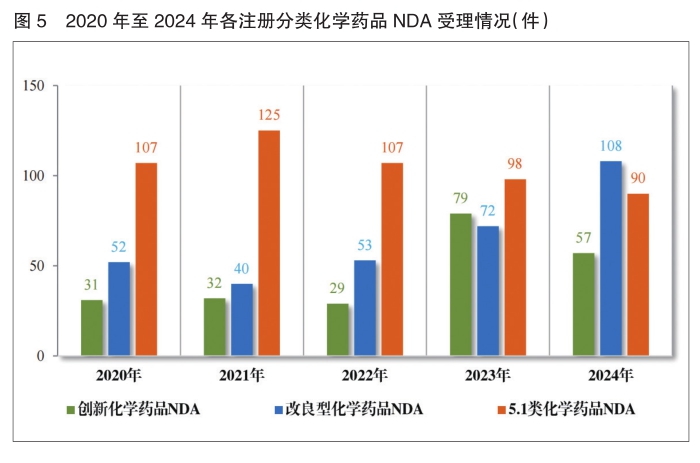
以注册分类统计,1785件IND中,包括创新化学药品IND 1345件(568个品种)、改良型化学药品IND 440件(237个品种);255件NDA中,包括创新化学药品NDA 57件(38个品种)、改良型化学药品NDA 108件(46个品种)、5.1类化学药品NDA 90件(57个品种)。
3.生物制品注册申请受理情况
2024年受理生物制品注册申请2447件,包括预防用生物制品注册申请239件、治疗用生物制品注册申请2201件和体外诊断试剂7件。
按注册申请类别统计,IND 1188件,NDA 254件,补充申请942件,境外生产药品再注册申请63件。
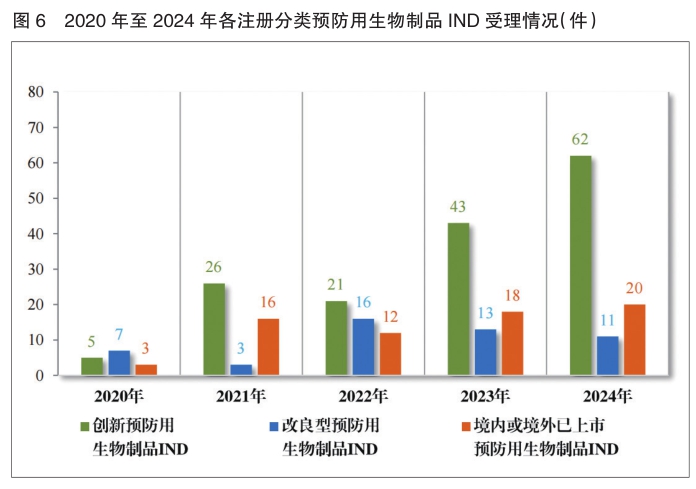
以注册分类统计,预防用生物制品IND 93件中,包括创新预防用生物制品IND 62件(41个品种)、改良型预防用生物制品IND 11件(8个品种)、境内或境外已上市预防用生物制品IND 20件(16个品种);预防用生物制品NDA 24件中,包括改良型预防用生物制品NDA 4件(3个品种)、境内或境外已上市预防用生物制品NDA 20件(14个品种)。
以注册分类统计,治疗用生物制品IND 1095件中,包括创新治疗用生物制品IND 879件(563个品种)、改良型治疗用生物制品IND 138件(65个品种)、境内或境外已上市治疗用生物制品IND 78件(43个品种)。
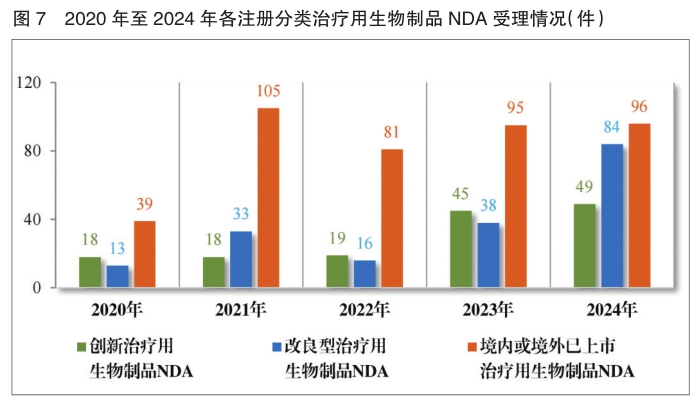
治疗用生物制品NDA 229件中,包括创新治疗用生物制品NDA 49件(33个品种)、改良型治疗用生物制品NDA 84件(42个品种)、境内或境外已上市治疗用生物制品NDA 96件(51个品种)。
(三)直接行政审批类注册申请受理情况
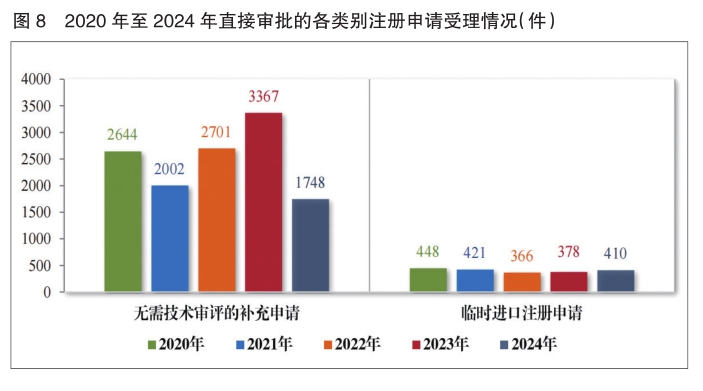
2024年受理直接行政审批类注册申请2158件,包括无需技术审评的补充申请1748件、临时进口注册申请410件。
第二章 药品注册申请审评审批情况
(一)总体情况
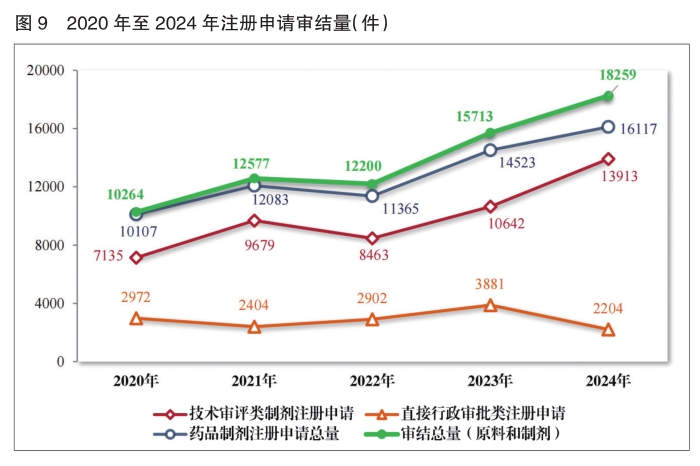
2024年,药审中心审结各类药品注册申请共18259件(同比增加16.20%),包括药品制剂注册申请16117件(同比增加10.98%)、化学原料药注册申请2142件(同比增加80.00%)。16117件药品制剂注册申请包含技术审评类注册申请13913件(同比增加30.74%)、直接行政审批类注册申请2204件。
截至2024年底,在审和待审的药品注册申请共12323件,其中包含原料药注册申请2130件;待申请人回复补充资料的注册申请共2239件,其中包含原料药注册申请587件。
(二)技术审评类注册申请审结情况
2024年审结的13913件技术审评类注册申请中,以药品类型统计,中药注册申请1907件,化学药品注册申请9759件,生物制品注册申请2247件。
以注册申请类别统计,2024年审结IND 3011件、验证性临床试验申请215件、NDA 439件、ANDA 3552件、一致性评价申请1135件、补充申请5090件、境外生产药品再注册申请471件。
2024年,药审中心以临床价值为导向,采取多种措施提高审评效率,加快新药好药上市,为患者提供更多的用药选择。
全年批准上市1类创新药48个品种,其中17个品种(35.4%)通过优先审评审批程序批准上市,11个品种(22.9%)附条件批准上市,13个品种(27.1%)在临床试验期间纳入了突破性治疗药物程序。
全年批准罕见病用药55个品种(未包括化学药品4类仿制药),其中20个品种(36.4%)通过优先审评审批程序加快上市,2个品种附条件批准上市。
全年批准儿童用药106个品种,包含71个上市许可申请,其中20个品种(18.9%)通过优先审评审批程序加快上市;另批准35个品种扩展儿童适应证。
全年批准境外已上市境内未上市的药品(化学药品5.1类、治疗用生物制品3.1类和预防用生物制品3.1类)89个品种,其中64个为首次批准上市,25个为已上市药品增加适应证。
1.中药注册申请审结情况
2024年审结中药注册申请1907件,按注册申请类别统计,IND 75件,NDA 16件,补充申请1808件,境外生产药品再注册申请8件。
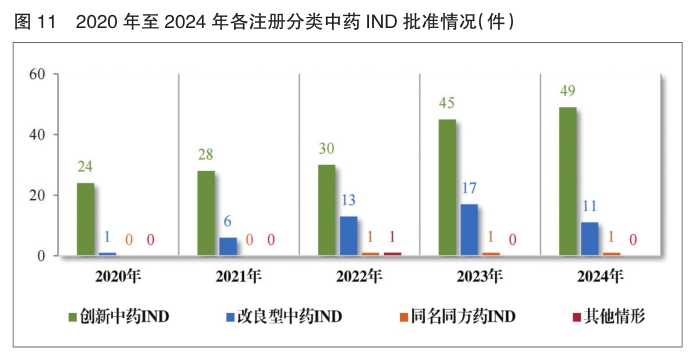
批准中药IND 61件(56个品种),以注册分类统计,包括创新中药IND 49件(44个品种)、改良型中药IND 11件(11个品种)、同名同方药IND 1件(1个品种);建议批准的中药NDA 14件(14个品种)中,包括创新中药NDA 3件(3个品种)、古代经典名方中药复方制剂NDA 11件(11个品种)。
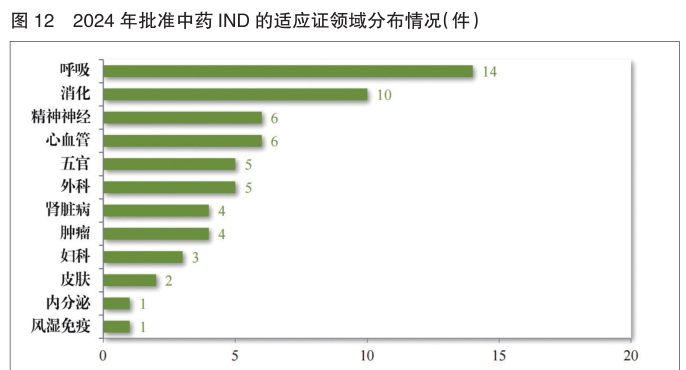
批准的61件中药IND中,涉及12个适应证领域,其中呼吸、消化药物较多,占中药IND批准量的39.34%。
建议批准的中药NDA 14件中,涉及6个适应证领域,其中呼吸药物较多,占中药NDA建议批准量的28.57%。
(下转3版)