□ 邸旭晨
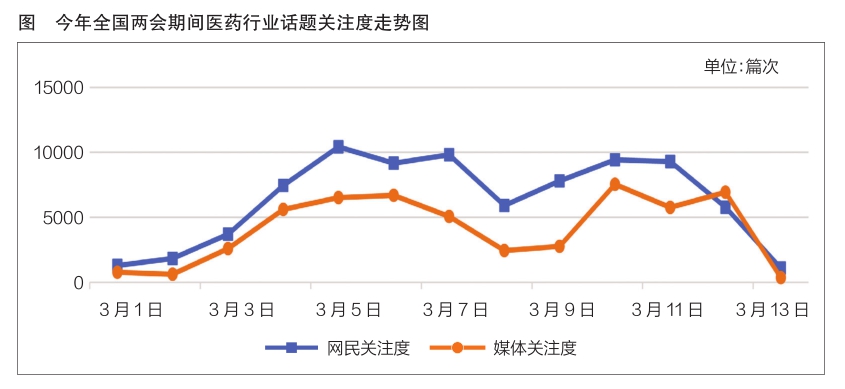
今年全国两会期间,代表委员对医药领域话题积极讨论,并建言献策。相关话题引发媒体和网民广泛关注,以3月1日至3月13日为监测时间段,如图所示,信息量传播走势呈“波浪式”。创新药械研发、中药传承创新、罕见病用药等话题舆论关注度较高。
话题一
持续鼓励创新药械研发
全国人大代表、荣昌生物制药(烟台)股份有限公司董事长王威东建议,出台对国谈创新药的倾斜支持政策,适当提高创新药医保支付经费占医保基金总量的比例。以患者获益和鼓励创新为导向,对临床价值高、患者急需的国产原研创新药,尤其是同类首创、同类最佳的创新药,加大医保基金预算。不断健全药品价格形成机制,积极支持高水平创新药获得合理回报,让真正的创新药企业收回研发成本,实现创新的良性循环,夯实可持续发展“支撑力”。
全国政协委员、中国心胸血管麻醉学会常务副会长敖虎山建议,进一步完善公立医院绩效考核机制与医保支付考核机制,出台有利于医院更积极使用创新产品的考核指标,并将研发成本纳入DRG/DIP的定价考量。同时,优化医保报销制度,对经科学验证的创新医疗产品适度提升报销额度。
全国政协委员、贝达药业股份有限公司董事长兼首席执行官丁列明建议,专项支持干细胞治疗等前沿领域的协同创新,增强政府引导基金与产业投资基金协作,合力支持创新药发展。
全国政协委员、复旦大学上海医学院副院长朱同玉建议,将目前现有对国产创新药的保护周期从3~5年进一步延长,让创新药企业能够收回研发成本。
话题二
中药传承创新
全国人大代表、中国工程院院士张伯礼建议,将“普药做实”,有些常用的中成药的安全性和效果已得到临床验证和广泛认可,这些普药可以转为OTC(非处方药),鼓励企业将这些OTC药品退出医保目录,直接在药店里按市场价销售;将“大药做强”,针对那些临床定位清晰、疗效较好、有独特优势的大品种中成药尽量多地纳入医保目录,同时应借助现代科技提升大品种中成药质量,并进行更深入的临床研究,强化循证医学依据。
全国人大代表、浙江中医药大学党委书记黄文秀建议,在条件成熟的高等中医药院校布局省级以上的中试平台和验证中心,提供专项资金用于设备升级和项目孵化,更好地解决利用中医药新技术、新装备规模化生产医疗机构制剂等问题,推动医疗机构制剂向中药新药转化,加快中药现代化进程。
全国人大代表、以岭药业董事长吴相君建议,分步建立国家级中医药数据平台,逐步建立健全中医药数据采集、传输、存储、处理、流通、使用的标准和规范,对中医药全产业链的数据进行整合,建立和完善国家级和区域中医药数据平台,实现中医药数据治理能力有效提升。同时,加快推进数智技术在新药研发中的应用,提升研发效率,借助数智技术推动中药材种植全生命周期数据的互联互通。
全国人大代表、内蒙古蒙药股份有限公司总工程师邢界红建议,国家相关部门组织对民族医药经典名方进行系统研究。通过对民族医药古籍的梳理、挖掘,将理论和经验转化为现代科学能够理解和验证的证据。建立民族医药经典名方数据库,整合各地民族医药经典名方,对组成、功效、临床应用、安全性、药材来源、炮制方法、传统用法用量等信息进行详细记录和分类管理。
全国人大代表、启迪药业集团股份公司董事长焦祺森建议,加强全国中药材统筹布局,如制定全国中药材产业发展中长期规划,明确各地区中药材种植、加工、研发等重点发展领域和方向,引导资源合理配置;加强对中药材质量的日常监督检查和抽检力度,严厉打击制售假劣中药材的违法行为;建立中药材质量信息发布平台,及时公布质量监测结果和市场监管情况。
全国政协委员、河北中医药大学校长郭毅建议,深入实施中药定量化研究,规范中药材从种子种苗繁育、种植养护、采收加工到仓储、物流和中药饮片炮制的全流程管理,健全中药全产业链标准体系;支持中药新药研发,加强中成药大品种培育,加速培育一批具有核心竞争力的名方大药和拳头产品;围绕强龙头、补链条、聚产业,鼓励中医药企业与高校、科研机构深入合作,打造现代化中医药产业园区。
话题三
罕见病药物可及
全国人大代表、中国医药投资有限公司董事、国药励展展览有限公司董事于清明建议,通过立法对罕见病预防、诊断和治疗体系的建设与管理,药品研发、生产与市场供应保障,医保政策与多元支付体系等作出相关要求。同时,强化罕见病防治的“三医”协同治理。加强药监、卫生健康、医保等多部门协同联动,制定罕见病药物研发生产与供应保障激励政策,如专项扶持资金、税收减免、优先审批、专利保护、数据保护、市场独占权等;明确罕见病诊疗体系建设标准与管理要求;统筹优化医保准入,探索实施多元化保障机制,切实提升罕见病医疗资源和药品可及性,真正实现罕见病医药创新激励制度化、患者权益保障稳定化、罕见病防治工作法治化。
全国人大代表、北京协和医院院长张抒扬建议,一是推动制定罕见病法律法规,加强我国在罕见病领域的法律及政策协同,明确各部门在罕见病防治中的职责;二是从国家层面设立罕见病专项基金,吸纳社会资金,加大对罕见病研究、药物研发和患者诊疗救助的投入;三是依托全国罕见病诊疗协作网,推动更多医疗机构应用罕见病人工智能辅助诊疗系统,提升识别诊治能力。
全国人大代表、中国工程院院士、哈尔滨医科大学党委书记张学建议,一是加强国家罕见病政策顶层设计和机构设置;二是明确罕见病定义,推进保障机制建设;三是加强“惠民保”对罕见病诊疗和用药保障力度;四是统筹引导慈善救助发挥更大作用。
话题四
强化药品监管
全国人大代表、好医生集团董事长耿福能建议,压实网络平台主体责任,强制相关网络平台接入AI审核系统,嵌入AI监测模块,对涉药商品名称、批准文号、包装图片等进行自动核验,未匹配商品一律禁止上架,对“中药代加工”“祖传秘方”等高风险关键词实施AI语义拦截,并有责任向监管部门举报。同时,实施信用惩戒制度。将纵容违法行为的平台纳入“药品安全黑名单”,限制其销售。对违规商家实施永久封禁,相关信息同步共享至市场监管征信系统。此外,尽快修订药品管理法实施条例,明确AI监测数据、取证的法律效力,规定平台未履行AI审核、日常管理义务的行政处罚条款。
全国人大代表、中南出版传媒集团编辑戴茵建议,建立绿色审批通道,简化适老化药品说明书的备案流程,推动适老化药品说明书尽快投放市场;将2006年发布的《药品说明书和标签管理规定》修订工作纳入议事日程,制定详细的实施细则,包括字号大小、语言表述、排版格式等,为企业提供明确的操作指南;建立全国统一的药品说明书电子信息平台,医药管理部门、药企、医院、药店、患者都可以借助该平台实现数字化需求;加大对药品说明书适老化改革的宣传力度,建立健全监督机制,对未按要求进行适老化改造的企业进行督促整改,确保改革措施落到实处。
全国政协委员、北京大学肿瘤医院副院长吴楠建议,针对过期药品回收处置管理,一是健全法律法规,建立长效协同机制,包括加快推动过期药品回收相关法律出台,明确责任主体,构筑过期药品回收联动平台,确定以政府部门为主体,药店、社区医疗机构、制药企业、社会组织或志愿团体等多部门协作的过期药品回收平台与工作机制;二是科学推进回收点设立与维护,强化回收管理,避免“无点可用”“设点难用”情况;三是规范药企生产行为,要求药品生产企业根据临床治疗需要进行药品包装设计,如短期治疗用药设计为药品含量少的小包装,基础病等慢性病治疗药品设计为药品含量多的大包装等;四是多途径强化居民用药宣传,提高居民参与回收过期药品的主动性。
话题五
加强医疗器械协同创新
全国人大代表,通用技术集团董事长、党组书记于旭波建议,设立国家重点专项,明确标志性医疗器械产品研发目标;组建创新联合体,推动协同创新和科研成果转化。同时,加大采购和金融支持力度,完善招标采购政策,支持国产医疗设备应用;拓宽融资渠道,支持企业创新发展。
全国人大代表,万华化学集团股份有限公司董事长廖增太建议,加强医疗器械关键原材料联合攻关机制,由国家有关部门牵头,通过对“卡脖子”的高端医用材料系统梳理,建立政、产、学、研、医全产业链联合攻关体,进一步加快高端医用材料国产化,并开设审核“绿色通道”。
全国人大代表、山东第一医科大学附属眼科医院院长史伟云建议,一是开通罕见医疗器械“研审联动”通道,企业可在Ⅰ期临床试验后提交有条件上市申请,技术审评时限缩短至40个工作日。对临床急需医疗器械实施“即收即检”,注册检验批次由3批减为1批。接受生物标志物、替代终点等间接疗效证据,豁免部分非关键临床试验。二是完善激励政策。对首个获批的罕见医疗器械给予5年市场独占期,其间不纳入集采范围。对延续生命类医疗器械实施“治疗IND”制度,允许审评期间有限使用,上市后5年内完成Ⅳ期临床追踪,未达标者启动退出机制。三是构建临床转化平台,在头部三甲医院设立国家罕见病医疗器械临床研究中心,配套远程手术指导系统;编制罕见病医疗器械临床应用指南等。
九三学社中央建议,推进“三医协同”,畅通“样品—产品—商品”的转化链条。一是“三医”联合制定创新医疗器械目录,建立衔接机制,让创新医疗器械在注册审批、临床应用、收费支付各环节“一绿到底”。二是把具有自主知识产权,特别是具有国际原创特性的高端医疗设备纳入各级医疗机构优先采购目录。
全国政协委员、中国科学院院士王建安建议,国家成立植入性医疗器械研发联盟,保护植入性医疗器械原始创新。此外,加快构建植入性医疗器械应用规范管理体系。
全国政协委员、京东集团技术委员会主席曹鹏建议,修订《医疗器械分类目录》,建立AI大模型医疗应用分级审批机制,对辅助诊断、健康管理等轻量化应用实行备案制管理,缩短相关产品审批周期,加快创新应用推广。
话题六
推动化妆品源头创新
全国人大代表、中国工程院院士李校堃认为,以生长因子为代表的生物活性多肽不仅具有广阔的国内国际市场前景,更能打造中国高端化妆品品牌和推动中国化妆品原料产业弯道超车。建议从政、产、学、研、用等维度上协同努力,建立一套科学规范、公开透明、对标国际通行规则的科学监管体系,积极推动生命科学、生物技术等化妆品原料相关领域的国际合作交流。
地方两会代表委员声音
1月起,地方两会陆续召开。各地方代表委员围绕医药领域的相关话题纷纷提出了一系列建议。
鼓励推广医疗机构制剂
上海市人大代表、上海市虹口区卫生健康委副主任邓小飞建议,上海市相关部门牵头制定政策,允许符合条件的医疗机构制剂在医联体内医疗机构之间流通使用,确保基层医疗机构能够使用上级医院的优质医疗机构制剂,提升基层诊疗水平,促进中医药资源的合理配置。流通的医疗机构制剂应满足5年以上的使用经验、良好的临床疗效和较少的不良反应等条件。
广东省政协委员、广州市知联会会长杨寿桃建议,明确将医疗机构制剂推广转化作为重点产业赛道,纳入生物医药产业发展规划统一布局,参照兄弟省市经验,尽快出台具体政策,为中药制剂研发、生产、转化提供有效指引和强力支持。充分利用“岭南名方”入选制剂可在广东全省及港澳地区调剂使用、医保支付、自主定价、纳入长期处方管理等政策,鼓励医疗机构将制剂委托院外生产运营,合作推广转化,造福更多百姓。
支持化妆品安全评估
上海市人大代表、美乐家中国区总裁许玮建议,一是鼓励政企协作,缩小化妆品原料安全数据缺口。对积极承担重难点原料安全评估工作的企业给予充分表扬和实质性政策扶持。二是加强化妆品原料安全评估人才培养。整合典型案例作为培训资源,定期组织企业安全评估人员进行培训指导。三是完善化妆品原料安全信息并动态调整原料数据库。推动上海市化妆品原料及品牌企业,充分利用并依托当前已建立的化妆品原料安全信息登记平台,持续丰富和强化安全信息数据,确保其时效性和准确性。同时,携手长三角各地监管部门,通过资源共享与协同合作,整合并发布与原料安全评估紧密相关的数据信息,为化妆品企业提供强有力的数据支撑和参考标准。 (夏晓雪)