第一章 药品注册申请受理情况
(一)总体情况
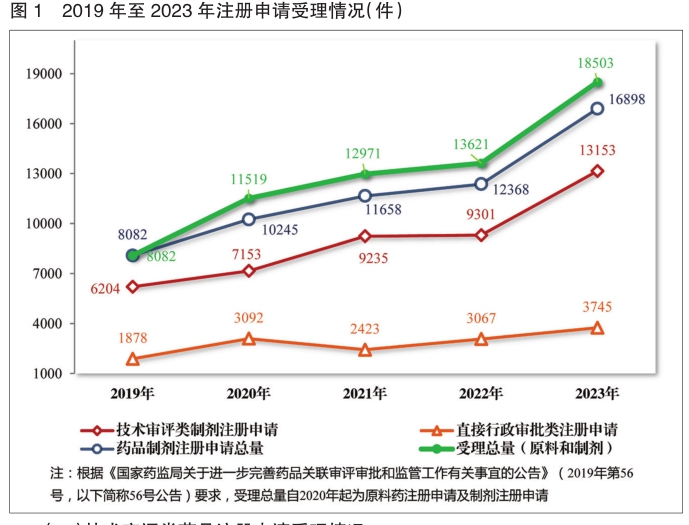
2023年,药品注册申请申报量持续增长,国家药监局药品审评中心(以下简称药审中心)受理各类注册申请18503件(同比增加35.84%,以受理号计,下同),包括药品制剂注册申请16898件(同比增加36.63%),化学原料药注册申请1605件(同比增加28.09%)。16898件药品制剂注册申请包括技术审评类注册申请13153件(同比增加41.41%,包括13144件药品,9件药械组合),直接行政审批类注册申请3745件(同比增加22.11%,包括补充申请和一次性进口)。
(二)技术审评类药品注册申请受理情况
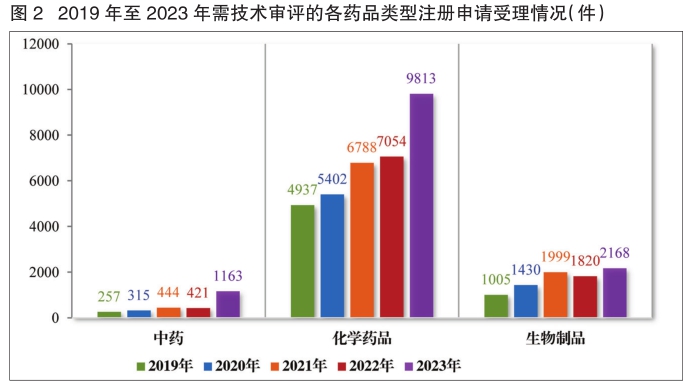
2023年受理的13144件技术审评类药品注册申请中,以药品类型统计,中药注册申请1163件,同比增加176.25%;化学药品注册申请9813件,同比增加39.11%,占全部需技术审评的药品注册申请受理量的74.66%;生物制品注册申请2168件,同比增加19.12%。
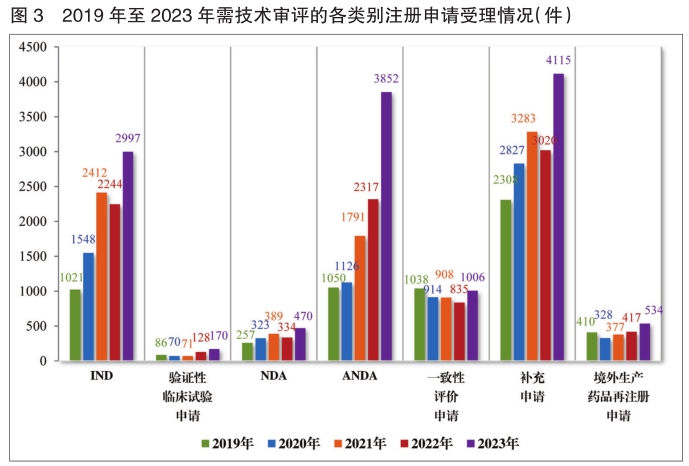
以注册申请类别统计,受理新药临床试验申请(该注册申请类别以下简称“IND”)2997件,同比增加33.56%;验证性临床试验申请170件,比2022年增加32.81%;新药上市许可申请(该注册申请类别以下简称“NDA”)470件,同比增加40.72%;同名同方药、化学仿制药上市许可申请(该注册申请类别以下简称“ANDA”)3852件,同比增加66.25%;仿制药质量和疗效一致性评价注册申请(该注册申请类别以下简称“一致性评价申请”)1006件,同比增加20.48%;补充申请4115件,同比增加36.26%;境外生产药品再注册申请534件,同比增加28.06%。
1.中药注册申请受理情况
2023年受理中药注册申请1163件。按审评序列统计,IND 75件,同比增加31.58%;NDA 26件,同比增加85.71%;补充申请1054件,同比增加206.40%;ANDA 1件,进口再注册7件,与去年持平。
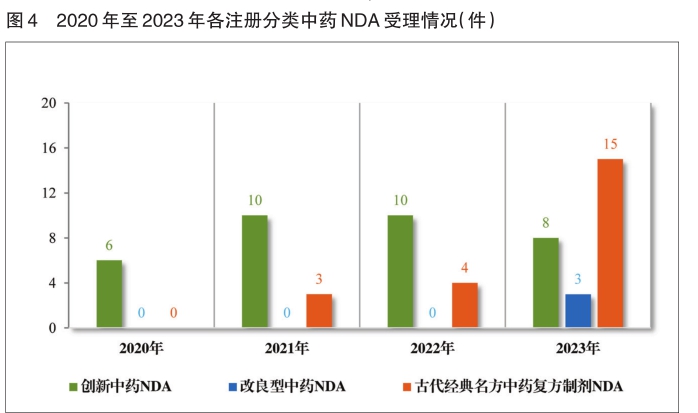
以注册分类统计,IND 75件,包括创新中药IND 54件(47个品种),同比增加38.46%;改良型中药IND 21件(21个品种),同比增加23.53%。NDA 26件,包括创新中药NDA 8件(7个品种),与上年持平;改良新中药NDA 3件(3个品种);古代经典名方中药复方制剂NDA 15件(11个品种),同比增加275.00%。
2.化学药品注册申请受理情况
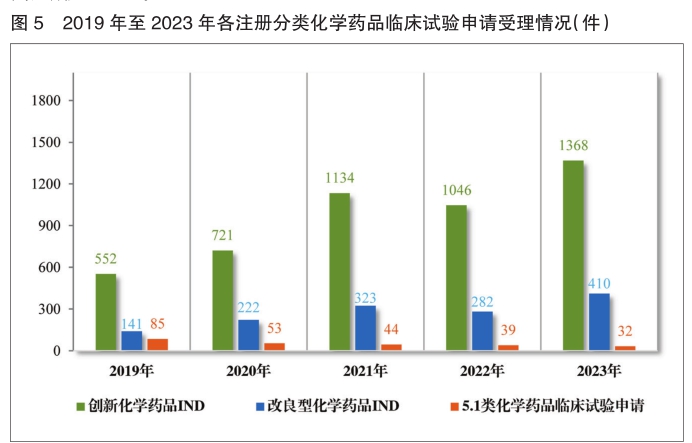
2023年受理需技术审评的化学药品注册申请9813件。按审评序列统计,IND 1778件,同比增加66.48%;NDA 249件,同比增加31.75%;ANDA 3854件,同比增加66.35%;一致性评价申请1006件,同比增加20.48%。5.1类化学药品注册申请130件,同比减少10.96%,其中验证性临床试验申请共32件,NDA 98件。
1778件IND中,包括创新化学药品IND 1368件(600个品种),同比增加30.78%;改良型化学药品IND 410件(229个品种),同比增加45.39%。NDA 249件中,包括创新化学药品NDA 79件(55个品种),同比增加172.41%;改良型化学药品NDA 72件(46个品种),同比增加35.85%;5.1类化学药品NDA 98件(62个品种),同比减少8.41%。
3.生物制品注册申请受理情况
2023年受理生物制品注册申请2168件,其中预防用生物制品注册申请189件,治疗用生物制品注册申请1969件,体外诊断试剂10件。
以注册申请类别统计,IND 1144件,同比增加33.18%;NDA 195件,同比增加48.85%;补充申请772件,同比增加0.65%;境外生产药品再注册申请57件,同比减少9.52%。
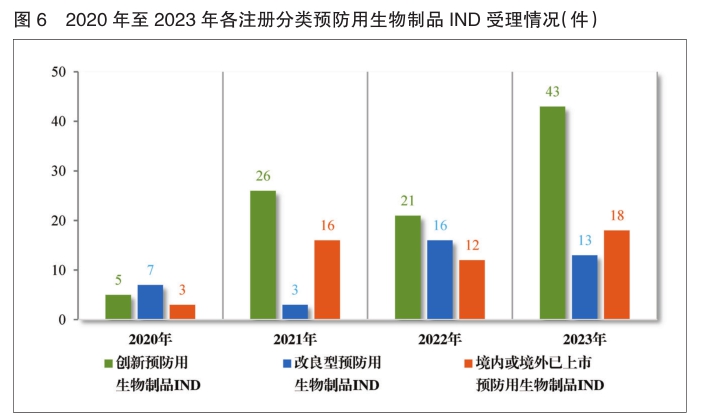
以注册分类统计,预防用生物制品IND 74件,包括创新预防用生物制品IND 43件(34个品种),同比增加104.76%;改良型预防用生物制品IND13件(11个品种),同比减少18.75%;境内或境外已上市预防用生物制品IND 18件(11个品种),同比增加50.00%。预防用生物制品NDA 17件,包括创新预防用生物制品NDA 1件(1个品种);改良型预防用生物制品NDA 2件(2个品种);境内或境外已上市预防用生物制品NDA 14件(6个品种)。
治疗用生物制品IND 1070件,包括创新治疗用生物制品IND 833件(576个品种),同比增加32.85%;改良型治疗用生物制品IND146件(75个品种),同比增加39.05%;境内或境外已上市治疗用生物制品IND 91件(46个品种),同比增加16.67%。
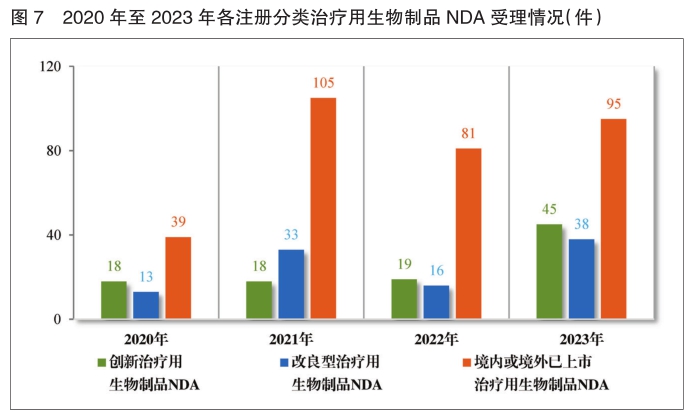
治疗用生物制品NDA 178件,包括创新治疗用生物制品NDA 45件(29个品种),同比增加136.84%;改良型治疗用生物制品NDA 38件(18个品种),同比增加137.50%;境内或境外已上市治疗用生物制品NDA 95件(58个品种),同比增加17.28%。
(三)直接行政审批类注册申请受理情况
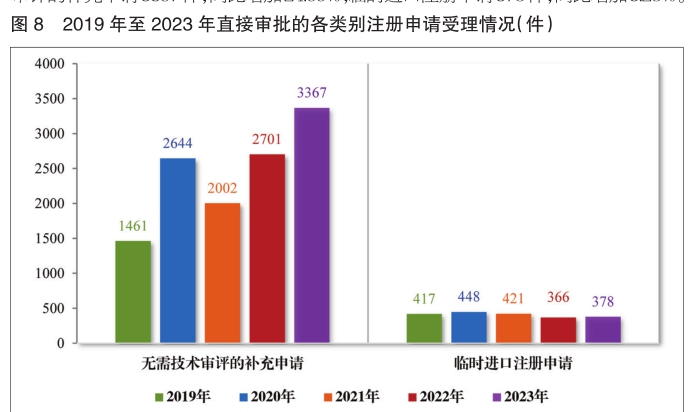
2023年受理直接行政审批类注册申请3745件,同比增加22.11%。包括无需技术审评的补充申请3367件,同比增加24.66%;临时进口注册申请378件,同比增加3.28%。
第二章 药品注册申请审评审批情况
(一)总体情况
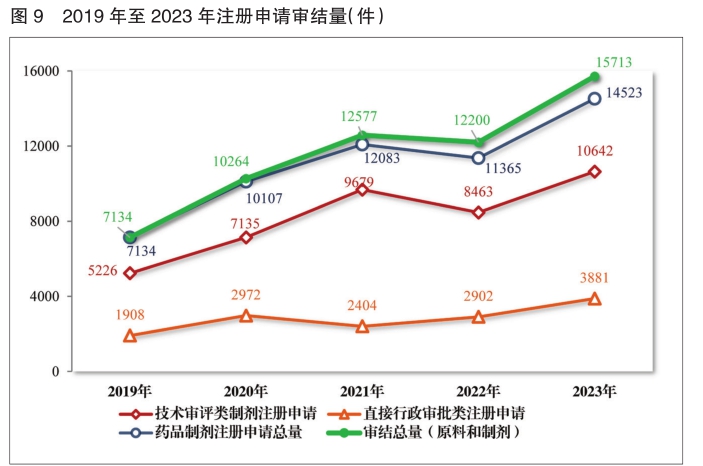
2023年,药审中心审结注册申请共15713件(同比增加28.80%),包括药品制剂注册申请14523件(同比增加27.79%),化学原料药注册申请1190件(同比增加42.51%)。14523件药品制剂注册申请包含技术审评类注册申请10642件(同比增加25.75%,包括10633件药品,9件药械组合),直接行政审批类注册申请3881件(同比增加33.74%)。
截至2023年底,在审和待审的注册申请共11059件,其中包含原料药注册申请2148件;待申请人回复补充资料的注册申请共2153件,其中包含原料药注册申请622件。
(二)技术审评类注册申请审结情况
2023年审结的10642件技术审评类注册申请中,按药品类型计,中药注册申请878件,同比增加131.05%;化学药品注册申请7725件,同比增加24.88%,占全部需技术审评审结量的72.59%;生物制品注册申请2030件,同比增加7.41%;药械组合注册申请9件。
按审评序列计,2023年审结IND 2724件,同比增加18.43%;验证性临床试验申请168件,同比增加22.63%;NDA 427件,同比增加26.71%;ANDA 2241件,同比增加60.76%;一致性评价申请990件,同比增加7.26%;补充申请3541件,同比增加20.03%;境外生产药品再注册申请538件,同比增加29.95%。
2023年,药审中心采取多种措施提高审评效率,加快药品审评速度,以临床价值为导向,为患者提供更多的用药选择。
全年批准上市1类创新药40个品种,其中9个品种(22.5%)通过优先审评审批程序批准上市,13个品种(32.5%)为附条件批准上市,8个品种(20%)在临床研究阶段纳入了突破性治疗药物程序、4个新冠治疗药物(10%)通过特别审批程序批准上市。
全年批准罕见病用药45个品种(未包括化药4类罕见病用药),其中15个品种(33.3%)通过优先审评审批程序得以加快上市,1个附条件批准上市。
全年批准儿童用药产品92个品种,包含72个上市许可申请,其中26个品种(28%)通过优先审评审批程序得以加快上市;另批准20个品种扩展儿童适应证,让更多儿童患者和千万家庭从中受益。
全年批准CAR-T细胞治疗产品3个,包括附条件批准伊基奥仑赛注射液、纳基奥仑赛注射液上市,附条件批准阿基仑赛注射液增加新适应证。
全年批准境外已上市、境内未上市的原研药品(化学药品5.1类、生物制品3.1类)86个品种,其中62个为新批准上市,包括1个纳入临床急需境外新药名单内的品种,24个为新增适应证。
1.中药注册申请审结情况
2023年审结中药注册申请878件,同比增加131.05%。按审评序列计,IND 77件,同比增长32.76%;NDA 21件,同比增加50.00%;ANDA 1件。
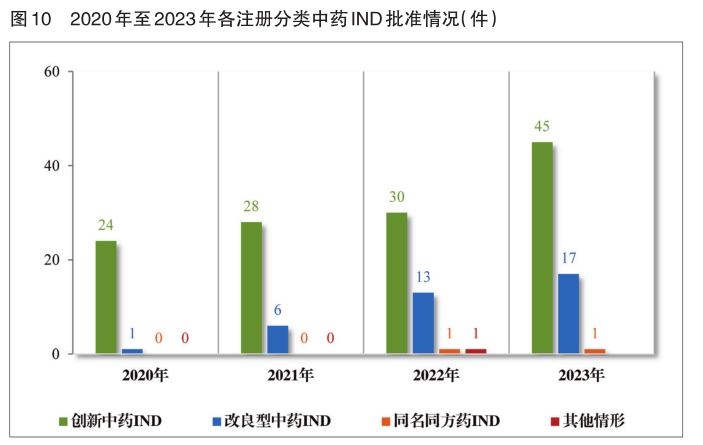
批准中药IND 63件,同比增长40.00%,包括创新中药IND 45件(39个品种),同比增长50.00%;改良型中药IND 17件(17个品种),同比增长30.77%;同名同方药IND 1件(1个品种)。建议批准中药NDA 11件(10个品种),同比增长37.50%,包括创新中药NDA 7件(6个品种);改良型中药NDA 1件(1个品种);古代经典名方中药复方制剂NDA 3件(3个品种)。建议批准中药ANDA 1件(1个品种),属中药同名同方药。
批准的63件中药IND中,涉及13个适应证领域,其中呼吸、消化药物较多,占中药IND批准量的46.03%。
建议批准的中药NDA 11件中,涉及6个适应证领域,其中消化药物较多,占中药NDA建议批准量的36.36%。
2.化学药品注册申请审结情况
2023年审结化学药品注册申请7725件,同比增加24.88%。按审评序列计,化学药品临床试验申请1762件,同比增加16.92%;化学药品NDA 237件,同比增加21.54%;化学药品ANDA 2240件,同比增加60.80%;化学药品一致性评价申请990件,同比增长7.26%。
(1)新药临床试验申请和新药上市申请
批准化学药品IND 1448件,同比增加15.92%,包括创新化学药品IND 1147件(513个品种),同比增加13.12%;改良型化学药品IND 301件(171个品种),同比增加27.54%。建议批准化学药品NDA186件(109个品种),同比增加21.57%,包括创新化学药品NDA 38件(20个品种),同比增加123.53%;改良型化学药品NDA 39件(25个品种),同比减少20.41%;5.1类化学药品NDA 109件(67个品种),同比增加31.33%。 (下转3版)