化妆品产业作为大健康产业的重要组成部分,其安全性(如过敏性、刺激性等)备受关注。目前,我国化妆品安全性评价方法以动物试验为主,随着动物“3R”(替代、减少、优化)原则被国际社会越来越广泛认可、化妆品动物试验禁令的持续推行,同时在科技发展的驱动下,动物替代试验方法在化妆品安全性评价领域受到越来越多的关注。
替代方法研究取得积极成效
在以欧盟为代表的化学品和化妆品法规推动下,动物替代试验方法成为热点研究领域,许多国家和地区均积极开发替代方法。同时,验证机构、标准化组织和监管机构也加快了对替代方法的研究和认可速度,近年来,除了经济合作与发展组织(OECD)验证认可的替代方法外,还有很多新方法正处于开发阶段或验证程序中。
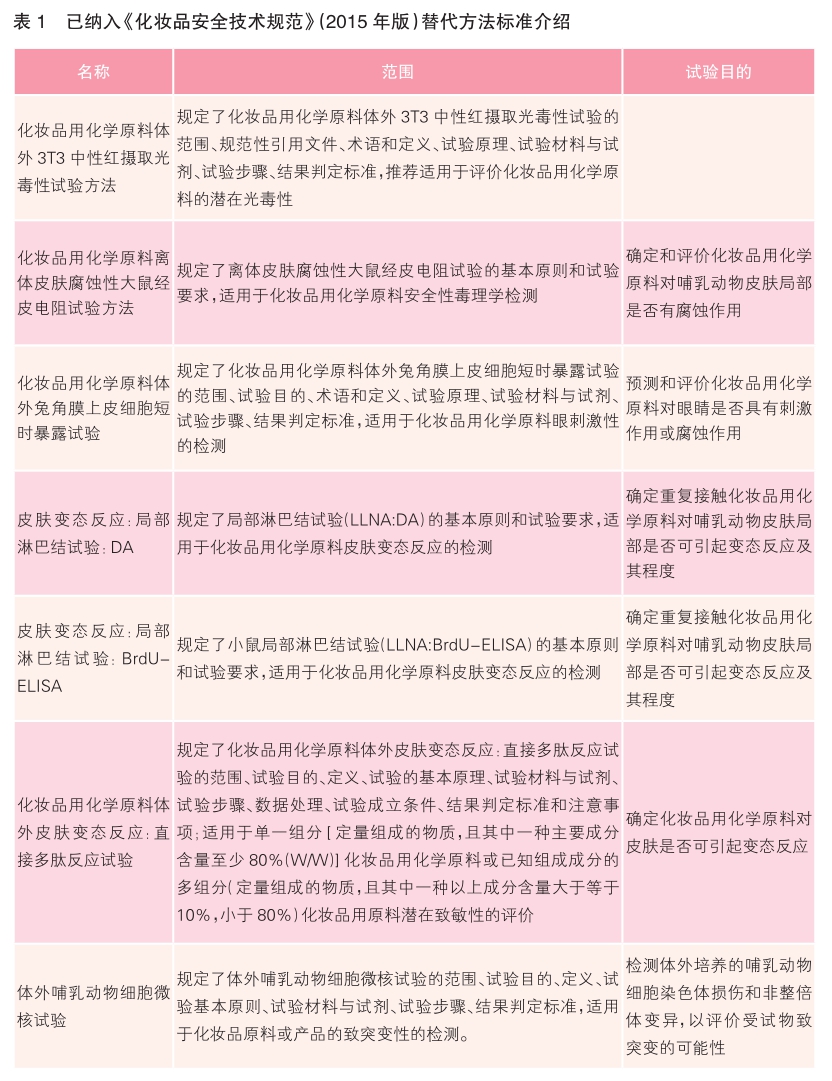
我国在化妆品动物替代试验方法标准认可方面紧随国际标准的发展趋势。2016年,《化妆品用化学原料体外3T3中性红摄取光毒性试验方法》被纳入《化妆品安全技术规范》(2015年版)(以下简称《规范》);2018年,中国食品药品检定研究院成立全国化妆品替代方法研究与验证工作组,并联合多家权威机构,进一步加快研究及验证化妆品替代检验方法。目前,被纳入《规范》的动物替代试验方法共7项,检验范围为化妆品用化学原料,与OECD测试指南一致;除2016年纳入的方法标准外,还包括《化妆品用化学原料离体皮肤腐蚀性大鼠经皮电阻试验方法》《化妆品用化学原料体外兔角膜上皮细胞短时暴露试验》《皮肤变态反应:局部淋巴结试验:DA》《皮肤变态反应:局部淋巴结试验:BrdUELISA》《化妆品用化学原料体外皮肤变态反应:直接多肽反应试验》和《体外哺乳动物细胞微核试验》(详见表1),有力推动了毒理学动物替代试验方法在我国化妆品安全性评价中的应用。
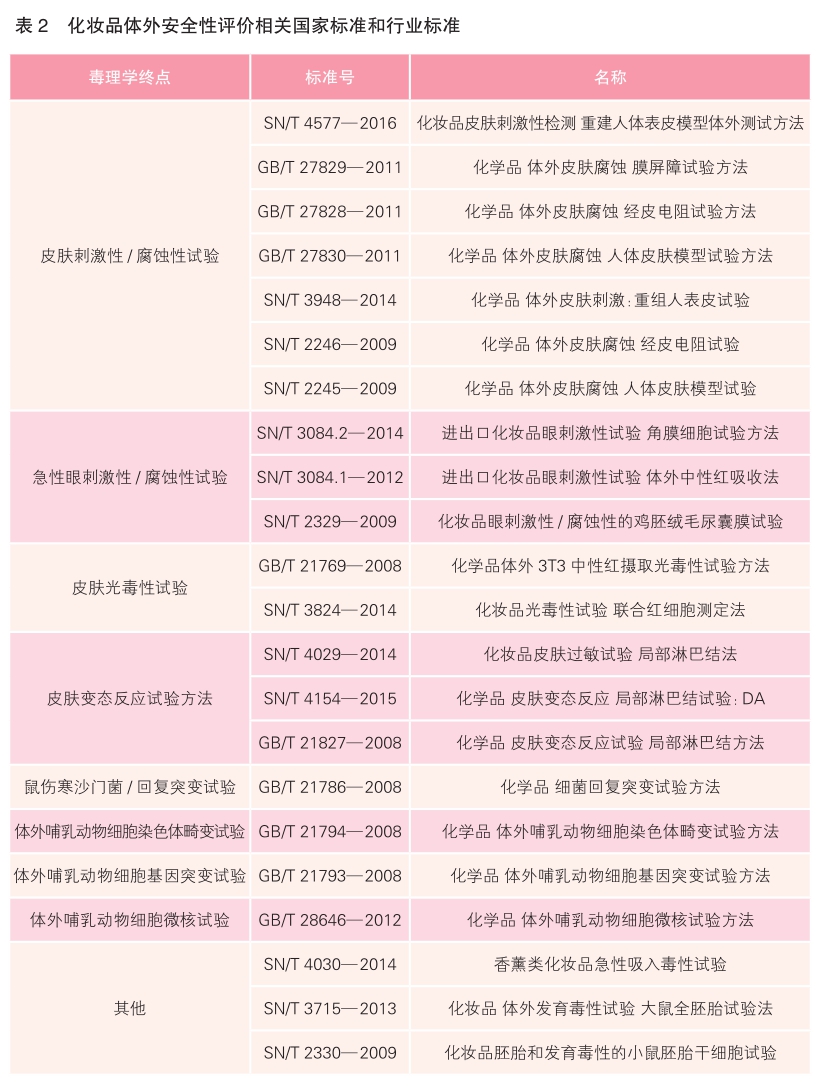
除被纳入《规范》的毒理学动物替代试验方法相关标准外,还有化妆品体外安全性评价相关系列国家标准和行业标准。据统计,共有相关标准22项,其中国家标准9项、行业标准13项(详见表2)。
研究仍面临问题和挑战
虽然国际上替代方法研究盛行,我国在该领域的研究也取得了积极进展,但由于种种原因,我国替代方法的研究和应用仍面临很多挑战,具体表现在以下几方面。
缺乏跨部门的国家级验证机构 很多国家和地区均组建了化妆品替代方法研究机构,如欧洲替代方法验证中心(ECVAM)、美国替代方法验证部门间协调委员会(ICCVAM)、欧洲动物替代试验方法合作组织(EPAA)、日本替代方法验证中心(JaCVAM)、韩国替代方法验证中心(KoCVAM)、巴西替代方法验证中心(BraCVAM)等。这些机构的设立对替代方法的开发、验证、认可起到了积极的推动作用,但我国尚未组建相关部门。
方法适用性待提升 在OECD测试指南中,替代方法可用于检测单一的化学物质或成分简单的混合物。在欧盟化妆品风险评估管理体系中,替代试验的检测对象主要是化妆品原料,OECD测试指南可以满足欧盟化妆品安全风险评估的要求。在我国,特殊化妆品上市前需要对终产品进行许可检验,而目前验证的替代方法不适用于化妆品产品。此外,我国化妆品原料中很多是动植物提取物,这类原料成分复杂、组分繁多,由这些原料混合成的化妆品产品形态复杂,不符合OECD指南中“化学物”的概念,无法用目前的替代方法为安全评估提供毒理学数据。因此,无论是基于我国化妆品法规对产品的检测要求,还是基于我国化妆品原料的特点,国际上通行的替代方法在转移至我国实际应用过程中,都需要进一步评估和确认其是否可以预测化妆品配方及产品安全性。
需探索全身毒性评价的替代方法 在化妆品安全性评价中,替代方法多集中于局部毒性评价,包括皮肤刺激性/腐蚀性、眼刺激性/腐蚀性、皮肤光毒性、皮肤致敏性等方法,而在全身毒性方面(致癌性/致畸性/致突变性、胚胎毒性等)缺乏相应替代方法。随着生物材料、微流控、组织工程和生物传感等技术的发展,器官芯片(OOC)在模拟人体不同组织器官主要空间结构和功能特征方面展现出巨大潜力。器官芯片通过控制细胞在体外培养过程中的生物学行为,在芯片上再现器官功能。可利用器官芯片研究不同器官和不同细胞之间的交互作用,开展安全性系统评价。
此外,较前沿的皮肤吸收、内分泌干扰等方面的替代方法研究在我国也相对较少。在组合策略方面,目前我国仍处于研究和建立单一方法的技术发展阶段,未来,组合策略的研究应用将成为重要课题。
三管齐下推进研究应用
我国在动物替代试验技术研究和方法推行方面起步较晚,结合上述问题和挑战,建议从三方面发力,进一步推进相关工作。
一是成立跨部门(如药监、环保、农业等部门)、跨学科(如药物毒理学、化妆品毒理学、化学品毒理学、农药毒理学)的联合验证工作组,统筹协调相关研究工作。
二是在化妆品安全性评价策略及新方法的开发验证方面,加快体外重组3D模型的研究,加强替代方法的研究技术储备,利用有害结局路径(AOP)理念,建立适应我国国情的替代方法;进一步制定相应技术指南,满足化妆品安全性评价及风险评估的要求。
三是器官芯片的构建和应用将是未来的发展方向,为全身毒性的体外评价提供新方案。建议加大力度推动我国器官芯片科学研究和产业化进展,使器官芯片这一新兴生物芯片技术在化妆品全身毒性评价中得以有效应用。
面向未来,随着替代技术的日益成熟,我国化妆品安全性评价将逐步缩小与发达国家和地区的差距,替代方法的技术水平也会相应提高,应用范围也将逐渐扩大,并将逐步实现自主创新,形成中国特色。
(本文摘编自中国健康传媒集团、中国药品监督管理研究会编写的《2021中国化妆品蓝皮书》,作者为谢珍、桑晶、何立成、匡荣)
相关链接
替代方法发展呈现三大趋势
近年来,化妆品动物替代试验方法发展呈现三大趋势。
一是有害结局路径(AOP)应用领域不断涌现新成果和新方法。每个AOP代表关于分子起始事件、中间事件和个体或群体水平的有害结局之间的联系。皮肤致敏的整合策略是首个成功应用AOP概念进行法规应用的案例,OECD已建立了皮肤致敏AOP框架并于2016年通过。该AOP包括四个关键事件:分子起始事件是化学物质(包括代谢物或非生物转化产物)与皮肤蛋白亲核性氨基酸残基的共价结合,为分子水平的表达;角质形成细胞的活化,为细胞水平的表达;树突状细胞(DC)的活化,为细胞水平的表达;T细胞活化和增殖,为组织器官层次的系统性表达。基于致敏产生机制,针对AOP顺序链上的关键事件设计相对应的致敏性检测方法。2014年,OECD发布了AOPWiki,借助互联网技术为AOP的开发提供高效共享、协调互补的平台。AOPWiki发布的有害结局和提出的关键事件,可为替代方法的开发提供新思路。
二是整合测试与评估方法(IATA)的开发。鉴于单一替代方法的不足和局限性,应合理、科学地组合使用单一方法,以获得毒理学全面评估。组合模式可参考OECD发布的I ATA指南。该指南不仅考虑现行有效的方法,还加入计算机预测方法、化学结构特征信息、人群暴露等。此外,对于复杂的毒性终点,也建议采用I ATA,以避免单一替代方法无法完整覆盖AOP全过程的局限,如可根据各单一方法的检验能力、灵敏度、局限性及使用条件等,将导致皮肤致敏发生的AOP不同阶段的替代方法组合起来,设计组合策略,提高致敏性风险预测的准确性。
三是安全评估推广应用。化妆品安全评估指利用已有的科学资料对化妆品中危害人体健康的已知或潜在的不良影响进行科学评价,能有效反映化妆品的潜在风险,是化妆品安全性评价的重要技术手段之一。国际上,欧盟、美国、日本等国家和地区已普遍将安全评估手段用于化妆品监管,建立了科学的评估工作程序,发布了指导性文件。近年来,化妆品安全评估理念在我国被广泛普及和应用。2010年,原国家食品药品监督管理局将安全风险评估概念引入对化妆品内可能存在的安全风险物质的管理中,标志着安全风险评估成为我国化妆品监管的科学方法之一。同年,原国家食品药品监督管理局印发《化妆品中可能存在的安全性风险物质风险评估指南》,明确化妆品中可能存在的安全性风险物质的风险评估程序。2013年,原国家食品药品监督管理总局印发《国产非特殊用途化妆品备案要求》,明确“国产非特殊用途化妆品风险评估结果能够充分确认产品安全性的,可免予产品的相关毒理学试验”。这既有助于确保化妆品安全,又能有效减少毒理学检测的安全风险评估方法的使用。2020年,《化妆品监督管理条例》出台,规定化妆品新原料和化妆品注册、备案前,注册申请人、备案人应当自行或者委托专业机构开展安全评估。2021年5月1日,《化妆品安全评估技术导则(2021年版)》正式施行,旨在规范和指导我国化妆品安全评估工作。