□ 刘颖慧 贺鑫鑫 曹进 路勇
化妆品安全报告是进行化妆品备案及申请注册过程中需要提交的重要资料性文件,提示产品安全性方面的主要关注点和评价内容。欧盟和我国化妆品法规均对化妆品安全报告作出相应要求,主要是表达产品在正常、合理、可预见的条件下对消费者是安全的。化妆品安全报告内容包括产品配方、原料、稳定性、安全评估等,为产品上市前审查和上市后监管提供依据和基础性资料。其中,化妆品稳定性是评价和回顾质量的重要依据之一。
化妆品安全性信息
总结评价原料及终产品MSDS信息
化妆品安全报告包括安全性信息和化妆品安全评估两部分。化妆品安全性信息主要针对化妆品原料及终产品相关化学品安全技术说明书(MSDS)信息进行总结评价,涵盖相应指标检测要求和结果。
化妆品配方的定量组成 配方标识需提供产品组成物质的化学名称、I NCI名称、CAS号、EINECS/ELINCS号等,并同时提交每个组成物质的百分含量。在安全评估中,对于物质范围含量,一般以高限进行计算;产品及原料中含有的防腐剂、抗氧化剂、螯合剂、缓冲剂、溶剂及添加剂等均应进行标注;对于香精或者芳香类物质,需要提供供应商所使用的名称,其安全性评估报告由生产商提供,并对其中的过敏性物质进行含量限制。
理化特性 化妆品安全报告中应包含原料和终产品的理化性质描述。原料理化性质包括化学鉴别、物理性状形式、分子量、溶解性、分配系数、物质纯度、高聚物的平均分子量以及范围。终产品的理化性质应包含产品质量指标,其指标值应给出范围,例如pH范围;还应给出在合理可预期贮存条件下的稳定性评估报告,该稳定性评估应在销售时的包装形式下进行,以帮助判断产品开封后的预期使用时间。
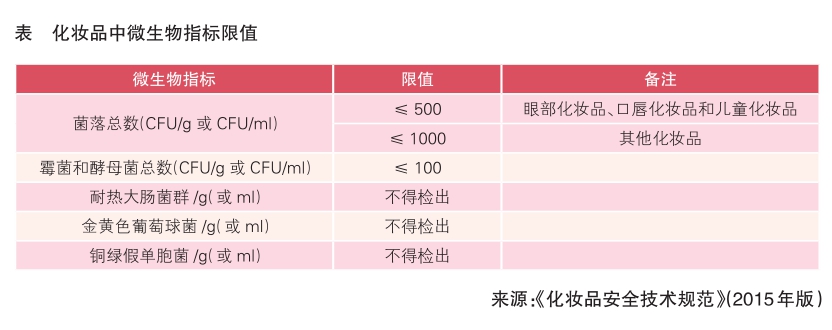
微生物指标 该部分主要对原料和终产品中可接受的微生物限度指标进行明确。我国《化妆品安全技术规范》(2015年版)对化妆品中微生物指标限值作出了具体规定(详见表)。欧盟将化妆品分为两个类别,一类是专为3岁以下儿童设计的或用于眼区和黏膜的产品,另一类适用于所有其他类别产品。欧盟规定,第一类产品需氧菌的总活菌数不应超过100CFU/g(或CFU/ml),第二类产品需氧菌的总活菌数不应超过1000CFU/g(或CFU/ml);1g(或1ml)的第一类和第二类化妆品中均不应检出铜绿假单胞菌、金黄色葡萄球菌和白色念珠菌。同时,考察产品中的微生物质量时,需要考虑是否需要对一些具有防腐成分的特殊产品进行测试,例如酒精含量高的产品、不含水的指甲油等;不与空气接触的产品(如气溶胶)和一次性使用的产品则不需要测试。
正常或可预期的用途 化妆品安全报告需要考虑产品的正常使用或可预见的使用情况,这样才能确认产品中成分的暴露程度。当确认了产品的正常使用和可预见的使用情况时,应在包装上标注相应警示语。
化妆品接触 需量化在正常和合理可预见的使用情况下,与人体外部部位(包括牙齿和口腔黏膜)接触的化妆品数量和使用频率。在适当情况下,应考虑次级暴露途径,例如吸入指甲油中的溶剂。化妆品安全报告需要考虑使用地点、使用面积、申请的产品数量、使用期限和频率、正常和合理可预见的暴露途径、目标(或暴露)人群、特定人群的潜在暴露、特殊人群(如3岁以下儿童)等。
体外接触 该类信息描述的目的是计算在正常和合理可预见的情况下使用,每个物质接触的人体外部部分、牙齿和黏膜情况。在产品使用过程中产生或释放的物质也应在化妆品安全报告中加以考虑。
毒理学概述 主要描述成品中每种物质的毒理学危害。毒理学概述需要考虑合适的终点,以证明成分是否安全。相关终点可能包括急性毒性、刺激和腐蚀性、皮肤刺激和皮肤腐蚀性、黏膜刺激(眼睛刺激)、皮肤敏感、皮肤/经皮吸收、重复剂量毒性、诱变/基因毒性、致癌性、生殖毒性、毒物动力学和光致毒性。在可能的情况下,需要确定没有观察到的不良反应水平(NOAEL),以便计算安全阈值。一般认为,在化妆品中使用的物质如果是安全的,其安全边际至少应为100。此外,毒理学概述中还应该考虑颗粒大小,特别是对于纳米颗粒。
不良影响和严重不良影响 产品投放市场后,应监测其安全性,并在必要时采取纠正措施。生产商或者监管人员应当建立收集、记录和确定不良影响原因的制度。任何不良影响和严重不良影响的信息都应包括在化妆品安全报告中。相关人员需要调查不良影响,以确定是否存在相关危害以及不确定的诱因;如有严重不良影响,应通知监管部门,并在化妆品安全报告中附送通知表格。
其他安全评估信息 包含其他与安全评估相关的信息,例如关于人类志愿者的研究。
化妆品安全评估
对产品安全性进行实际评估
化妆品安全评估是对产品安全性的实际评估。
化妆品安全评估应给出对产品是否安全的合理意见。评估结论应说明产品在正常和可预见的使用情况下是否安全,是否影响人体健康;如果评估认为产品不安全,则产品不能投放市场。
此外,化妆品安全评估还应给出标签警示和使用说明,以及关于专业使用产品的预防性信息。为评估化妆品是否影响人体健康安全、是否符合相关规定要求,评估人员应确保拥有所有相关信息,并解释是如何根据安全性信息得出结论的。评估应考察配方中成分的安全性和成品的安全性。如果存在对现有安全评估结果产生影响的关于所使用物质的新科学发现和毒物学数据,如原料配方或规格发生变化、使用条件发生变化、在合理可预见的使用条件下存在滥用等情况,应对评估结论进行修改。
(摘编自《日用化学品科学》2022年第2期)