2月9日—2月15日,医药行业的这些动态值得关注。
行业政策动态
1 国务院新闻办公室举行政策例行吹风会,介绍深化药品和高值医用耗材集中带量采购改革进展情况。会议指出,国务院常务会议决定常态化、制度化开展药品和高值医用耗材集中带量采购,进一步降低患者医药负担。
2 国家药监局发布《舒筋定痛片中松香酸检查项补充检验方法》《保胎灵(片、胶囊)中牛皮源成分检查项补充检验方法》《阿胶强骨口服液中牛皮源成分检查项补充检验方法》《龟鹿补肾片中牛皮源成分检查项补充检验方法》《清热解毒口服液中灰毡毛忍冬皂苷乙检查项补充检验方法》等5项补充检验方法。
3 国家药监局发布仿制药参比制剂目录(第五十一批),涉及注射用头孢比罗酯钠等药品。
4 国家药监局药品审评中心(CDE)发布《生物类似药临床药理学研究技术指导原则》,提出生物类似药临床药理学研究的指导性建议。指导原则阐述了生物类似药临床药理学研究的具体内容及相关要求,涉及药代动力学和药效动力学研究的研究设计、评价指标、统计分析和接受标准等,临床药理学研究中的安全性和免疫原性考虑,以及申报资料要求。该指导原则适用于结构和功能明确的治疗用重组蛋白质制品,并提示对聚乙二醇等修饰的产品及抗体偶联药物类产品等按生物类似药研发时应慎重考虑。
5 CDE再次对《化学原料药受理审查指南(试行)(征求意见稿)》公开征求意见。本版征求意见稿将适用范围调整为化学原料药上市申请,对登记资料中登记号赋予原则、证明文件内容进行调整,新增工艺验证资料等内容的提交要求,并对光盘中文件格式及大小等予以规范。
6 CDE发布《对我国〈以药动学参数为终点评价指标的化学药物仿制药人体生物等效性研究技术指导原则〉中关于多规格豁免BE药学评价标准“处方比例相似性”相关问题的问答(试行)》,以规范和指导化学药物仿制药的研究和开发,促进多规格豁免BE的药学研究和评价工作。
产品研发上市信息
1 国家药监局附条件批准辉瑞公司新冠病毒治疗药物奈玛特韦片/利托那韦片组合包装(即Paxl ovid)进口注册。该品为口服小分子新冠病毒治疗药物,用于治疗成人伴有进展为重症高风险因素的轻至中度新型冠状病毒肺炎(COVID-19)患者,例如伴有高龄、慢性肾脏疾病、糖尿病、心血管疾病、慢性肺病等重症高风险因素的患者。患者应在医师指导下严格按说明书用药,使用中应高度关注说明书中列明的与其他药物相互作用信息。
2 国家药监局发布4期药品批准证明文件待领信息,共包括214个受理号,涉及再鼎医药(上海)有限公司等企业。
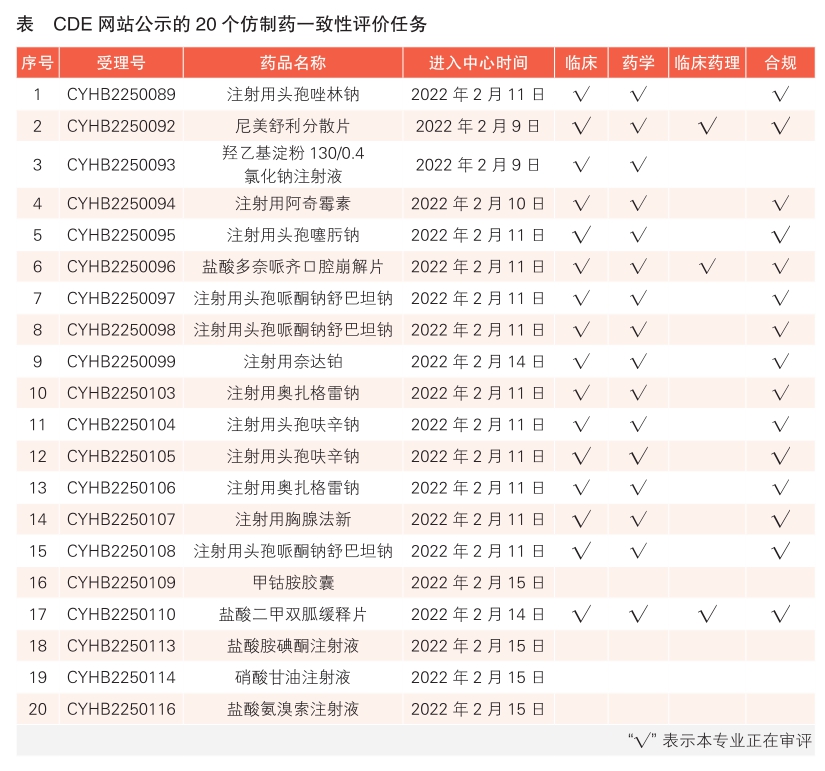
3 CDE网站公示20个仿制药一致性评价任务,涉及注射用头孢唑林钠等药品。
4 CDE承办受理43个新药上市申请,包括人源TH-SC01细胞注射液等药品。
医药企业观察
1 美国食品药品管理局(FDA)召开肿瘤药物咨询委员会(ODAC)会议,对信达生物与礼来制药合作的PD-1抗体信迪利单抗注射液的新药上市申请(BLA)审评问题进行讨论并投票。结果认为,信迪利单抗应该补充临床试验才能获得批准。
2 信达生物与驯鹿医疗共同宣布,美国FDA授予两家公司共同开发的全人源自体BCMA CAR-T注射液(研发代号为IB1326/ CT103A)孤儿药资格,用于治疗复发/难治性多发性骨髓瘤(R/R MM)。
3 普利制药发布公告称,收到美国FDA签发的注射用艾司奥美拉唑钠仿制药上市批准通知、荷兰药物评价委员会(CBG)批准注射用艾司奥美拉唑钠的技术审评报告的通知,全资子公司浙江普利收到CBG批准奥卡西平片的技术评审通知。
4 博腾股份发布公告称,收到辉瑞旗下Pf izer I r el and Pharmaceut ical s的新一批采购订单,博腾股份将为其提供合同定制研发生产(CDMO)服务。截至该公告披露日,博腾股份新获得订单金额合计6.81亿美元,超过其最近一个会计年度经审计营业收入的50%。
5 华东医药全资子公司中美华东制药与AKSO Biopharmaceutical宣布达成战略合作。根据协议,中美华东制药将获得后者开发的在研产品AB002(用于实体瘤治疗)在亚太地区(除日本)的独家临床开发及商业化权益,此项合作总金额最高可达7500万美元。
6 博雅辑因与Arbor Biotechnologies公司达成全球非独占许可协议,以利用后者的CRISPR基因编辑技术,开发针对肿瘤的特定体外细胞疗法。
7 百洋医药与上海谊众签署合作协议,双方将就上海谊众旗下肿瘤创新药物注射用紫杉醇聚合物胶束的商业化开展合作,共同推进国产肿瘤创新药物可及性。
8 贵州百灵与重庆市潼南区中医院签订技术开发(合作)合同,双方将共同开发糖宁通络片。
药品集中采购
1 四川省医保局就《关于开展部分医保药品支付标准试点工作的通知(征求意见稿)》公开征求意见。征求意见稿提出将29种药品纳入医保支付标准试点范围。原则上该省所有定点医疗机构和定点零售药店,由医保基金支付试点药品费用时,均拟适用此通知确定的医保支付标准。
2 江苏省医保局发布《关于调整国家医保谈判药品“双通道”管理及单独支付药品名录的通知》,明确将硫培非格司亭注射液调出“双通道”管理及单独支付名录,且对沙库巴曲缬沙坦钠片治疗原发性高血压适应症不实行“双通道”管理及单独支付。 (刘思慧整理)